题目内容
10.苯作萃取剂,并用分液漏斗萃取溴水中的溴单质的实验,下列说法正确的是( )| A. | 不能使用酒精作为萃取剂,因为溴单质在酒精中的溶解度比在水中的小 | |
| B. | 静置分层后有色层在下层,水层几乎无色 | |
| C. | 分液漏斗使用前应当用蒸馏水检验是否漏液 | |
| D. | 振荡、静置分层后,依次用两个不同的烧杯从下口分别接取上下两层液体 |
分析 A.酒精与水不分层;
B.苯的密度比水小;
C.有活塞或瓶塞的装置,使用前需要检查是否漏水;
D.下层液体下口流出,上层液体从上口倒出.
解答 解:A.酒精与水不分层,不能选用酒精作为萃取剂,故A错误;
B.苯的密度比水小,有色层在上层,故B错误;
C.分液漏斗有塞子和活塞使用前应先检查是否漏水,故C正确;
D.下层液体下口流出,上层液体从上口倒出,以免污染液体,故D错误.
故选C.
点评 本题考查化学实验的基本操作,题目难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
17.常温常压下,等物质的量的下列物质所占有的最大体积的是( )
| A. | MgO | B. | FeCl2 | C. | CO | D. | H2O |
18. 已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
(1)写出碳酸的第一步电离平衡常数表达式:Ka1=$\frac{c({H}^{+})•c(HC{{O}_{3}}^{-})}{c({H}_{2}C{O}_{3})}$.
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:H2CO3>HSO3->HCO3-.
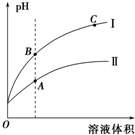
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化图象中,曲线I表示的酸是CH3COOH(填化学式).
②a、b、c三点中,水的电离程度最大的是C(填字母).
 已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:| 醋酸 | 碳酸 | 亚硫酸 |
| Ka=1.75×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:H2CO3>HSO3->HCO3-.
(3)如图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化图象中,曲线I表示的酸是CH3COOH(填化学式).
②a、b、c三点中,水的电离程度最大的是C(填字母).
5.下列说法正确的是( )
| A. | 液态 HCl、固体NaCl 均不导电,所以 HCl、NaCl 均是非电解质 | |
| B. | NH3、CO2的水溶液均导电,所以 NH3、CO2 均是电解质 | |
| C. | 铜、石墨均导电,所以它们是电解质 | |
| D. | 蔗糖、酒精在水溶液或熔化时均不导电,所以它们是非电解质 |
2.想一想:盐酸、75%的酒精溶液、氯水这些物质为什么归为一类,下列哪些物质还可以和他们归为一类( )
| A. | H2SO4 | B. | 胆矾 | C. | Fe(OH)3胶体 | D. | 液氯 |
19.下列物质的转化过程须加氧化剂的是( )
| A. | CuO→Cu | B. | MnO4-→Mn2+ | C. | Na2SO3→Na2SO4 | D. | Cl2→Cl- |
20.在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为原来的60%,则( )
| A. | 平衡向逆反应方向移动了 | B. | 物质A的转化率增大了 | ||
| C. | 物质B的质量分数减小了 | D. | a>b |
 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
 .
. +4NaOH$→_{△}^{H_{2}O}$
+4NaOH$→_{△}^{H_{2}O}$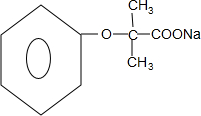 +3NaCl+2H2O.
+3NaCl+2H2O. .
.