题目内容
6.漂白粉在空气中易失效的原因是( )| A. | CaCl2易吸收空气中的水分 | |
| B. | Ca(ClO)2见光易分解 | |
| C. | Ca(ClO)2与空气中的水分和二氧化碳作用,生成HClO | |
| D. | Ca(ClO)2易被空气中的氧气氧化 |
分析 漂白粉的有效成分为Ca(ClO)2,由于HClO的酸性比碳酸弱,Ca(ClO)2易与空气中的CO2和H2O反应生成次氯酸,次氯酸不稳定,易分解.
解答 解:次氯酸酸性小于碳酸,次氯酸钙和二氧化碳、水反应生成次氯酸,次氯酸不稳定,光照易分解,导致漂白粉失效,反应方程式为Ca(ClO)2+C02+H20=2HClO+CaC03、2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+02↑,
A.氯化钙不是漂白粉的有效成分,吸收水蒸气不变质,故A错误;
B.次氯酸钙见光不分解,故B错误;
C.Ca(ClO)2与空气中的水分和二氧化碳作用,生成HClO,次氯酸见光分解,使漂白粉变质,故C正确;
D.次氯酸钙是强氧化剂不能被空气中的氧气氧化,故D错误;
故选C.
点评 本题考查次氯酸钙的性质,为高频考点,侧重双基的考查,题目难度不大,注意HClO的酸性、不稳定性是决定漂白粉失效的主要原因.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.下列关于化学键的叙述正确的是( )
| A. | 化学键存在于原子之间,也能存在于分子与离子之间 | |
| B. | 两个原子之间的相互作用叫做化学键 | |
| C. | 离子键是阴、阳离子之间的吸引力 | |
| D. | 化学键通常指的是任意两个或多个原子之间强烈的相互作用 |
17.电子计算机所用钮扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e═ZnO+H2O和Ag2O+H2O+2e═2Ag+2OH-;下列判断正确的是( )
| A. | 锌为正极,Ag2O为负极 | B. | 锌为负极,Ag2O为正极 | ||
| C. | 原电池工作时,Ag2O发生氧化反应 | D. | 原电池工作时,负极区溶液PH增大 |
14.下列化学用语正确的是( )
| A. | 甲烷的结构式:CH4 | B. | 溴乙烷的分子式CH3CH2Br | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 苯的最简式 CH |
1.关于0.01mol•L-1NaHCO3溶液,下列说法正确的是( )
| A. | 溶质水解反应:HCO3-+H2O?H3O++CO32- | |
| B. | 离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) | |
| C. | 微粒浓度关系:c(Na+)═2[c(H2CO3)+c(HCO3-+c(CO32-)] | |
| D. | 微粒浓度关系:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
11.X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第ⅥA族.
(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式).
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有Cl2、O3、ClO2(写出其中两种物质的化学式).
(4)ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑.
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一.元素E位于第四周期,与元素Y同主族.在如表中列出对H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中E用元素符号表示)
(6)由碳元素(C)、Y和M三种元素组成的化合物CYM中,所有原子的最外层都满足8电子结构.写出该化合物的电子式(电子式中Y、M用元素符号表示)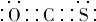 .
.
请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第ⅥA族.
(2)上述元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式),非金属气态氢化物还原性最强的是H2S(写化学式).
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有Cl2、O3、ClO2(写出其中两种物质的化学式).
(4)ZX与水反应放出气体的化学方程式为NaH+H2O=NaOH+H2↑.
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一.元素E位于第四周期,与元素Y同主族.在如表中列出对H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中E用元素符号表示)
| 编号 | 性质推测 | 化学方程式 |
| 示例 | 氧化性 | H2EO3+4HI═Z↓+2I2+3H2O |
| 1 | ||
| 2 |
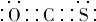 .
.
18.许多国家十分重视海水资源的综合利用,不需要化学变化就能从海水中获得的物质是( )
| A. | Cl2 | B. | Na | C. | 淡水 | D. | NaOH |
15.下列措施一定能使化学反应速率加快的是( )
| A. | 增大反应物的量 | B. | 增大压强 | C. | 升高温度 | D. | 使用催化剂 |
 由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂.如:
由氧化物经氯化作用生成氯化物是工业生产氯化物的常用方法,Cl2、CCl4是常用的氯化剂.如: ,其中碳氧原子之间共价键是c(填序号):
,其中碳氧原子之间共价键是c(填序号):