题目内容
6.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜 | |
| B. | 标准标况下,33.6 L三氧化硫中含有1.5NA个三氧化硫分子 | |
| C. | 1 mol Cl2与过量的铁反应,转移3NA个电子 | |
| D. | 1 mol FeCl3跟水反应,完全转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
分析 A、电解精炼铜时,阴极反应为:Cu2++2e-=Cu;
B、标况下三氧化硫为固体;
C、氯气和铁反应后变为-1价;
D、一个氢氧化铁胶粒是多个氢氧化铁的聚集体.
解答 解:A、电解精炼铜时阳极电极反应:Cu-2e-═Cu2+,Fe-2e-═Fe2+,Zn-2e-═Zn2+,Ni-2e-═Ni2+,阴极电极反应为Cu2++2e-═Cu,若阴极得到电子数为NA个,依据电子守恒,则阴极析出32 g铜,故A正确;
B、标准状况下,三氧化硫不再是气体,不能用气体摩尔体积计算,故B错误;
C、1 mol Cl2与过量的铁反应后变为-1价,故1mol氯气转移2NA个电子,故C错误;
D、氢氧化铁胶体粒子是氢氧化铁形成的集合体,故胶粒数一定小于NA,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
16.分子式为C4H8O2并能发生水解反应的有机物(不含立体异构)有( )
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
17.将下列物质分别加入溴水中,溴水颜色不变浅的是( )
| A. | KCl晶体 | B. | H2S气体 | C. | CCl4 | D. | Mg |
1.由我国已故著名化学实业家吴蕴初先生创办的上海天原化工厂,目前生产的液氯中含Cl299.9%,含水量小于0.05%,该化工厂生产的液氯应该是( )
| A. | 纯净物 | B. | 混合物 | C. | 化合物 | D. | 单质 |
11.羟氨苄青霉素是高效、广谱和低毒的抗生素,其结构简式如图所示.下列说法错误的是( )

| A. | 羟氨苄青霉素在空气中不能很稳定地存在 | |
| B. | 每个羟氨苄青霉素分子中含有3个手性碳原子 | |
| C. | 羟氨苄青霉素既能与盐酸反应,又能与碳酸氢钠溶液反应 | |
| D. | 羟氨苄青霉素可以与FeCl3发生显色反应 |
18.下列有关金属及其化合物的说法正确的是( )
| A. | 铝和氢氧化钠溶液反应生成Al(OH)3和Na | |
| B. | 钠在空气中燃烧生成淡黄色的NaO2 | |
| C. | 铁在高温下与水蒸气反应生成Fe3O4和H2 | |
| D. | 用碳酸钠和氢氧化钙反应制NaHCO3 |
15.CaO+H2O=Ca(OH)2的反应类型属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
9.下列各种冶炼方法中,可制得相应金属的为( )
| A. | 加热氧化镁 | B. | 电解熔融氧化铝 | ||
| C. | 电解氯化钠溶液 | D. | 氯化钠与铝粉高温共热 |


 +HO-NO2$→_{△}^{浓H_{2}SO_{4}}$
+HO-NO2$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. .
. (写出其中一种的结构简式).
(写出其中一种的结构简式).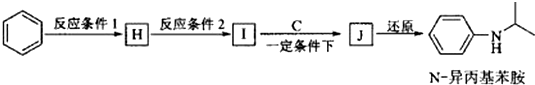
 .
.