题目内容
18.下列有关金属及其化合物的说法正确的是( )| A. | 铝和氢氧化钠溶液反应生成Al(OH)3和Na | |
| B. | 钠在空气中燃烧生成淡黄色的NaO2 | |
| C. | 铁在高温下与水蒸气反应生成Fe3O4和H2 | |
| D. | 用碳酸钠和氢氧化钙反应制NaHCO3 |
分析 A.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气;
B.钠在空气中燃烧生成淡黄色的过氧化钠;
C.高温下铁与水蒸气反应生成四氧化三铁和氢气;
D.碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠.
解答 解:A.铝的活泼性比钠弱,金属铝不可能置换出钠,铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,故A错误;
B.钠化学性质活泼,在空气中燃烧生成Na2O2,故B错误;
C.在高温下Fe能够与水水蒸气反应生成Fe3O4和H2,故C正确;
D.用碳酸钠和氢氧化钙反应制NaOH,无法获得NaHCO3,故D错误;
故选C.
点评 本题考查了常见金属及其化合物性质,题目难度不大,明确常见元素及其化合物性质为解答关键,注意铁在高温下与水反应生成的是四氧化三铁,不是氧化铁,为易错点.

练习册系列答案
相关题目
8.下列离子方程式书写不正确的是( )
| A. | FeCl2溶液中通入Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | FeS固体放人稀硝酸溶液中:FeS+2H+═Fe2++H2S↑ | |
| D. | AlCl3溶液中加入过量氨水:Al3++3NH3•H20═Al(OH)3↓+3NH4+ |
6.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜 | |
| B. | 标准标况下,33.6 L三氧化硫中含有1.5NA个三氧化硫分子 | |
| C. | 1 mol Cl2与过量的铁反应,转移3NA个电子 | |
| D. | 1 mol FeCl3跟水反应,完全转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
13.有6种物质:①乙烷;②乙烯;③苯;④邻二甲苯;⑤聚乙烯;⑥环己烯.其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
| A. | ①③⑤ | B. | ②③⑤ | C. | ①④⑥ | D. | ③④⑤ |
3.某同学设计原电池装置如图所示,下列说法正确的是( )
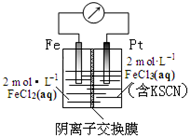

| A. | 电子由铁极经溶液向铂极迁移 | |
| B. | 放电过程中交换膜右侧溶液颜色逐渐变浅 | |
| C. | 正极的电极反应式为Fe3++3e?=Fe | |
| D. | 若转移1mol e-,交换膜左侧溶液中则减少1 molCl- |
1.下列相关的说法不正确的是( )
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 工业粉尘中含有Pb、Cd、Cr、V、As等金属元素,过量摄入均对人体有害 | |
| C. | 用工业明胶制作用药胶囊,会导致过量Cr元素摄入人体而提高致癌风险 | |
| D. | 分光光度计通过测定溶液颜色分析反应物(或生成物)浓度变化,从而确定化学反应速率 |
 某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验.
某中学化学兴趣小组同学为探究元素周期律,设计了如下一系列实验. CH3COOCH2CH3+H2O已知:乙醛可氧化为乙酸(该方程式不用写)
CH3COOCH2CH3+H2O已知:乙醛可氧化为乙酸(该方程式不用写)