题目内容
药物E具有抗癌抑菌功效,其合成路线如图所示:
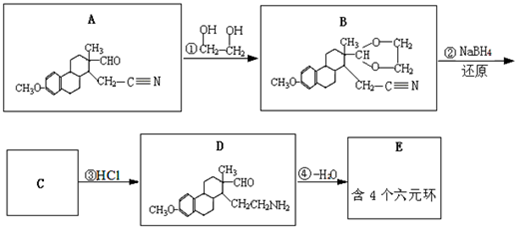
已知:NaBH4是一种很强的还原剂,可以将-C≡N还原为-CH2NH2.
(1)关于化合物D的说法错误的是 .
a.1mol D最多可与3mol H2发生加成反应 b.可以与盐酸发生反应
c.可以使高锰酸钾酸性溶液褪色 d.是烃的含氧衍生物
(2)反应③在水溶液中进行,HCl是催化剂,此反应中除了生成D外,还有一种产物,该产物的名称是 .
(3)E的结构简式为 .
(4)合成路线中设计反应①和③的目的是 .
(5)阅读以下信息,依据以上流程图和所给信息,以CH3CHO和CH3NH2为原料设计合成α-氨基丙酸[CH3CH(NH2)COOH]的路线.已知: (提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A→B→C…→H.)
(提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A→B→C…→H.)

已知:NaBH4是一种很强的还原剂,可以将-C≡N还原为-CH2NH2.
(1)关于化合物D的说法错误的是
a.1mol D最多可与3mol H2发生加成反应 b.可以与盐酸发生反应
c.可以使高锰酸钾酸性溶液褪色 d.是烃的含氧衍生物
(2)反应③在水溶液中进行,HCl是催化剂,此反应中除了生成D外,还有一种产物,该产物的名称是
(3)E的结构简式为
(4)合成路线中设计反应①和③的目的是
(5)阅读以下信息,依据以上流程图和所给信息,以CH3CHO和CH3NH2为原料设计合成α-氨基丙酸[CH3CH(NH2)COOH]的路线.已知:
 (提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A→B→C…→H.)
(提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A→B→C…→H.)考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)根据D的结构简式,其含有苯环、醛基、氨基来判断;
(2)B生成C的反应为还原反应,-C≡N生成-CH2NH2,则C为 ,D为
,D为 ,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式分析;
,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式分析;
(3)D生成E为脱水反应生成六元环,-CHO和-CH2NH2生成-C=N-;
醛基被以氧化和还原,性质活泼,在反应中往往要保护官能团;
(4)醛基被以氧化和还原,性质活泼,在反应中往往要保护官能团;
(5)根据题给信息,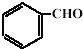 和
和 反应生成
反应生成 ,然后与HCN发生加成反应生成
,然后与HCN发生加成反应生成 ,然后在酸性条件下可生成目标物.
,然后在酸性条件下可生成目标物.
(2)B生成C的反应为还原反应,-C≡N生成-CH2NH2,则C为
 ,D为
,D为 ,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式分析;
,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式分析;(3)D生成E为脱水反应生成六元环,-CHO和-CH2NH2生成-C=N-;
醛基被以氧化和还原,性质活泼,在反应中往往要保护官能团;
(4)醛基被以氧化和还原,性质活泼,在反应中往往要保护官能团;
(5)根据题给信息,
 和
和 反应生成
反应生成 ,然后与HCN发生加成反应生成
,然后与HCN发生加成反应生成 ,然后在酸性条件下可生成目标物.
,然后在酸性条件下可生成目标物.解答:
解:(1)根据D的结构简式,其含有苯环、醛基、氨基,所以
a.因为含有苯环、醛基,所以1mol D最多可与4mol H2发生加成反应,故a错误;
b.因为含有氨基,具有碱性,则可以与盐酸发生反应,故b正确;
c.因为含有醛基,所以可以使高锰酸钾酸性溶液褪色,故c正确;
d.因为含有氨基,所以不是烃的含氧衍生物,故d错误;
故选:ad;
(2)B生成C的反应为还原反应,-C≡N生成-CH2NH2,则C为 ,D为
,D为 ,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式还有一种产物,该产物的名称是乙二醇,故答案为:乙二醇;
,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式还有一种产物,该产物的名称是乙二醇,故答案为:乙二醇;
(3)D生成E为脱水反应生成六元环,-CHO和-CH2NH2生成-C=N-,E为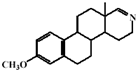 ,故答案为:
,故答案为: ;
;
(4)醛基在有机合成中易被氧化和还原,故应先保护,而后释放出来,故答案为:保护醛基不被还原;
(5)CH3CHO和CH3NH2反应生CH3CH=NCH3,然后与HCN发生加成反应生成CH3C(CN)-NHCH3,然后在酸性条件下可生成目标物,反应流程为 ,
,
故答案为: .
.
a.因为含有苯环、醛基,所以1mol D最多可与4mol H2发生加成反应,故a错误;
b.因为含有氨基,具有碱性,则可以与盐酸发生反应,故b正确;
c.因为含有醛基,所以可以使高锰酸钾酸性溶液褪色,故c正确;
d.因为含有氨基,所以不是烃的含氧衍生物,故d错误;
故选:ad;
(2)B生成C的反应为还原反应,-C≡N生成-CH2NH2,则C为
 ,D为
,D为 ,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式还有一种产物,该产物的名称是乙二醇,故答案为:乙二醇;
,根据反应③在水溶液中进行,HCl是催化剂,结合C和D的结构简式还有一种产物,该产物的名称是乙二醇,故答案为:乙二醇;(3)D生成E为脱水反应生成六元环,-CHO和-CH2NH2生成-C=N-,E为
 ,故答案为:
,故答案为: ;
;(4)醛基在有机合成中易被氧化和还原,故应先保护,而后释放出来,故答案为:保护醛基不被还原;
(5)CH3CHO和CH3NH2反应生CH3CH=NCH3,然后与HCN发生加成反应生成CH3C(CN)-NHCH3,然后在酸性条件下可生成目标物,反应流程为
 ,
,故答案为:
 .
.
点评:本题考查有机物的合成,题目难度中等,解答本题的关键是根据官能团的结构、性质以及物质之间反应的官能团的转化判断可能发生的反应类型,准确把握题给信息.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列化学用语表达正确的是( )
A、碳-12原子
| ||
B、N2电子式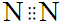 | ||
| C、次氯酸的结构式 H-Cl-O | ||
D、硫离子结构示意图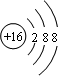 |
用标准的氢氧化钠溶液(指示剂为酚酞)滴定某未知浓度的盐酸,以下操作造成测定结果偏低的是( )
| A、配制标准溶液所用的氢氧化钠已经潮解 |
| B、滴定终点读数时,俯视滴定管的刻度,其它操作均正确 |
| C、未用标准液润洗碱式滴定管 |
| D、盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
实验室需配制 100mL 1.5mol/L NaOH 溶液,下列叙述正确的是( )
| A、转移液体时,玻璃棒应紧靠容量瓶口 |
| B、容量瓶上标有温度、浓度、容积和压强 |
| C、将所需的6.0g氢氧化钠固体倒入到容量瓶中溶解 |
| D、定容时若俯视刻度线观察液面,会使所配制的NaOH 溶液的浓度偏高 |
已知某温度下0.1moL/L的NaHB溶液中c(H+)>c(OH-),则下列关系式一定正确的是( )
| A、c(H+)+c(Na+)=c(HB-)+c(B2-)+c(OH-) |
| B、c(Na+)=0.1 moL/L≥c(B2-) |
| C、c(H+)×c(OH-)=1×10-14 |
| D、溶液的pH=1 |
在强酸性溶液中,离子能大量共存的组别是( )
| A、Na+、K+、OH-、Cl- |
| B、Al3+、SO42+、Na+、Cl- |
| C、Na+、Ba2+、Cl-、SO42- |
| D、Na+、Ca2+、HCO3-、Cl- |

 为原料合成重要的化工产品
为原料合成重要的化工产品 .合成路线流程图示例如下:
.合成路线流程图示例如下: .
.