��Ŀ����
5�� ���ڿ��淴Ӧ2A������+B��g��?2C��g������ͼ����������һ��ʱ��Ӧ��C�İٷֺ�����ѹǿ�Ĺ�ϵ���ߣ��ش��������⣺
���ڿ��淴Ӧ2A������+B��g��?2C��g������ͼ����������һ��ʱ��Ӧ��C�İٷֺ�����ѹǿ�Ĺ�ϵ���ߣ��ش��������⣺��1������A��״̬�����壨����塱����Һ�塱���塱����
��2��ͼ��a��b��c��d�ĵ��б�ʾδ�ﵽƽ��״̬��v����v���ĵ���a��
��3����a��b��c���������´�ƽ��ʱ��v��a����v��b����v��c�����ɴ�С����v��b����v��a����v��c����
��4������2SO2��g��+O2��g��?2SO3��g������H=-198kJ/mol����ʵ�����������У�ԭ������SO2Ϊ7%�������������O2Ϊ11%����ѹ�½��У������¶���450�����ң�
����ԭ������SO2��O2������Ȳ���2��1����Ҫ7��11����Լ2��3����ԭ����Ϊ������SO2��ת���ʣ�����ں��������У���������82%���������塰����������Ƿ���СSO2��ת���ʲ��ᣨ��ᡱ���ᡱ����
���� ��1������ͼ����Ϣ����֪��������ѹǿ��C�ĺ������ӣ����Կ����ж�AΪ���壻
��2������ͼ�еĸ������֪��a�㴦�������Ϸ������Կ����жϴ�ʱC��Ũ�ȹ�������Ӧ�����淴Ӧ�ķ����ƶ���
��3������ͼ����Ϣ����֪��b��C��Ũ����������a��Ũ����С��Ϊc�����Դﵽƽ���������Ϊb�㣬��СΪc�㣻
��4��������������ڻ�������еı����ܹ����Ӷ��������ת���ʣ������������ݻ����䣬���������������ܵ��ķ�ѹǿ���䣬ƽ�ⲻ�ƶ������Ծݴ˽����⣮
��� �⣺��1��������ƽ����ϵ��ѹǿ��ƽ���ƶ��Ľ��Ӧʹ��ϵ��ѹǿ��С����ƽ�������������С�����ƶ�����ͼ����Ϣ����֪����ѹǿ����C�ĺ������ӣ����Կ����ж�AΪ���壬
�ʴ�Ϊ�����壻
��2������ͼ�еĸ������֪��a�㴦�������Ϸ������Կ����жϴ�ʱC��Ũ�ȹ�������Ӧ�����淴Ӧ�ķ����ƶ���ѡ��a��
�ʴ�Ϊ��a��
��3������ͼ����Ϣ����֪��b��C��Ũ����������a��Ũ����С��Ϊc�����Դﵽƽ���������Ϊb�㣬��СΪc�㣬��v��b����v��a����v��c����
�ʴ�Ϊ��v��b����v��a����v��c����
��4��������������ڻ�������еı����ܹ����Ӷ��������ת���ʣ������������ݻ����䣬���������������ܵ��ķ�ѹǿ���䣬ƽ�ⲻ�ƶ���
�ʴ�Ϊ��Ϊ������SO2��ת���ʣ����ᣮ
���� ���⿼���˻�ѧƽ��Ӱ�����ط�����ͼ������Ӧ�ã���ɳ����ԭ�����漰ƽ������������Ҫ��һ��ԭ�����������е�ƽ���ƶ������ⶼ��������������ԭ�������ͺ��жϣ���ȷӦ�õ�ǰ��������������ԭ���ı��ʺ��ں�����Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | KNO3 K2SO4 K2CO3 K3PO4 | B�� | NaOH KOH Ba��OH��2 Ca��OH��2 | ||
| C�� | Na2O K2O CaO CO2 | D�� | HNO3 H2SO4 H3PO4 HClO3 |
| A�� | NO2-���������� Na2O2-���������� Al2O3-���������� | |
| B�� | Ư��-����� ����-������ HD-���� | |
| C�� | ����-�� ����-�� С�մ�-��ʽ�� | |
| D�� | ����-ǿ����� ���ᱵ-ǿ����� ����-������� |
��Al Fe ��C Si ��Cu H2 ��H2 Cu��
| A�� | ֻ�Т٢� | B�� | ֻ�Тڢ� | C�� | ֻ�Т٢ڢ� | D�� | �٢ڢۢ� |

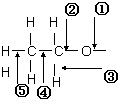 �Ҵ������и���ѧ����ͼ��ʾ��
�Ҵ������и���ѧ����ͼ��ʾ��