题目内容
15.下列各组单质中,前者能将后者从化合物中置换出来的是( )①Al Fe ②C Si ③Cu H2 ④H2 Cu.
| A. | 只有①② | B. | 只有②④ | C. | 只有①②④ | D. | ①②③④ |
分析 能发生置换反应的种类有:金属置换金属(溶液中或固态)、金属置换非金属、非金属置换金属、非金属置换非金属,据此分析解答.
解答 解:①铝和铁的氧化物能发生铝热反应而制取铁,所以能发生置换反应,故①正确;
②C和二氧化硅在高温下反应生成Si和CO,所以C能把Si置换出来,故②正确;
③Cu与非氧化性酸不反应,不能置换出酸中的氢气,故③错误;
④氢气能还原氧化铜得到铜,所以能发生置换反应,故④正确;
故选C.
点评 本题考查了置换反应能否发生的判断,明确物质之间发生置换反应的种类是解本题关键,能举出离子即可解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.从有机化合物的分类来看,下列反应中的X属于( )
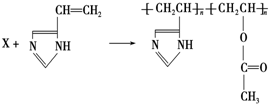

| A. | 醇 | B. | 烷烃 | C. | 烯烃 | D. | 酯 |
4.SO2通过下列工艺流程可制得化工业原料H2SO4和清洁能源H2.
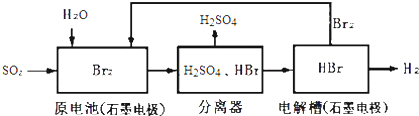
(1)根据资料:
为检验分离器的分离效果,取分离后的H2SO4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到无淡黄色沉淀产生,最终生成白色沉淀,证明分离效果较好.
(2)表示该工艺流程的总反应化学方程式为:SO2+2H2O=H2SO4+H2;该生产工艺的优点有溴可以循环利用,获得清洁能源氢气(答一点即可).
(3)某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol•L-1,加入等体积的溴化钠溶液,若要产生溴化银沉淀,加入的溴化钠溶液的最小浓度是10-3mol•L-1.

(1)根据资料:
| 化学式 | Ag2SO4 | AgBr | AgCl |
| Ksp | 1.4×10-5 | 5.0×10-13 | 1.8×10-10 |
(2)表示该工艺流程的总反应化学方程式为:SO2+2H2O=H2SO4+H2;该生产工艺的优点有溴可以循环利用,获得清洁能源氢气(答一点即可).
(3)某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol•L-1,加入等体积的溴化钠溶液,若要产生溴化银沉淀,加入的溴化钠溶液的最小浓度是10-3mol•L-1.
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,16gO3中含氧原子数为NA | |
| B. | 2.3g Na与足量O2反应转移的电子数为NA | |
| C. | 0.1mol•L-1 Na2CO3溶液中含钠离子数为0.2NA | |
| D. | 标准状况下,2.24 L四氯化碳中含碳原子数为0.1NA |
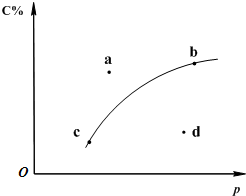 对于可逆反应2A(?)+B(g)?2C(g);如图是其它条件一定时反应中C的百分含量与压强的关系曲线.回答下列问题:
对于可逆反应2A(?)+B(g)?2C(g);如图是其它条件一定时反应中C的百分含量与压强的关系曲线.回答下列问题: