题目内容
下列结论错误的是( )
①微粒半径:K+>Al3+>S2->Cl-
②氧化性:Cl2>S>Se>Te
③氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
④非金属性:O>N>P>Si
⑤离子的还原性:S2->Cl->Br->I-
⑥酸性:H2SO4>H3PO4>H2CO3>HClO.
①微粒半径:K+>Al3+>S2->Cl-
②氧化性:Cl2>S>Se>Te
③氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
④非金属性:O>N>P>Si
⑤离子的还原性:S2->Cl->Br->I-
⑥酸性:H2SO4>H3PO4>H2CO3>HClO.
| A、①③④ | B、①⑤ |
| C、②④⑤ | D、①②⑥ |
考点:微粒半径大小的比较,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:①电子层结构相同,核电荷数越大离子半径越小,电子层越多,离子半径越大;
②非金属性越强,单质的氧化性越强;
③非金属性越强,其氢化物稳定性越强;
④同周期自左而右非金属性增强,同主族自上而下非金属性减弱;
⑤非金属性越强,阴离子还原性越弱;
⑥非金属性越强,元素最高价含氧酸的酸性越强,HClO的酸性弱于碳酸.
②非金属性越强,单质的氧化性越强;
③非金属性越强,其氢化物稳定性越强;
④同周期自左而右非金属性增强,同主族自上而下非金属性减弱;
⑤非金属性越强,阴离子还原性越弱;
⑥非金属性越强,元素最高价含氧酸的酸性越强,HClO的酸性弱于碳酸.
解答:
解:①K+、S2-、Cl-电子层结构相同,核电荷数越大离子半径越小,Al3+离子电子层最少,离子半径最小,故离子半径:S2->Cl->K+>Al3+,故①错误;
②同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性Cl>S>Se>Te,非金属性越强,单质的氧化性越强,故氧化性:Cl2>S>Se>Te,故②正确;
③非金属性F>Cl>S>P>Si,非金属性越强,其氢化物稳定性越强,故氢化物的稳定性:HF>HCl>H2S>PH3>SiH4,故③正确;
④同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性:O>N>P>Si,故④正确;
⑤非金属性:Cl>Br>I>S,非金属性越强,阴离子还原性越弱,故离子的还原性:S2->I->Br->Cl-,故⑤错误;
⑥非金属性:S>P>C,非金属性越强,元素最高价含氧酸的酸性越强,故酸性H2SO4>H3PO4>H2CO3,HClO的酸性弱于碳酸,故⑥正确,
故选B.
②同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性Cl>S>Se>Te,非金属性越强,单质的氧化性越强,故氧化性:Cl2>S>Se>Te,故②正确;
③非金属性F>Cl>S>P>Si,非金属性越强,其氢化物稳定性越强,故氢化物的稳定性:HF>HCl>H2S>PH3>SiH4,故③正确;
④同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性:O>N>P>Si,故④正确;
⑤非金属性:Cl>Br>I>S,非金属性越强,阴离子还原性越弱,故离子的还原性:S2->I->Br->Cl-,故⑤错误;
⑥非金属性:S>P>C,非金属性越强,元素最高价含氧酸的酸性越强,故酸性H2SO4>H3PO4>H2CO3,HClO的酸性弱于碳酸,故⑥正确,
故选B.
点评:本题考查元素周期律,难度中等,注意对元素周期律的理解掌握,有利于基础知识的巩固.

练习册系列答案
相关题目
已知H2S在水溶液中分两步电离:
第一步:H2S?H++HS- K1=
=1.3×10-7;
第二步:HS-?H++S2- K2=
=7.1×10-15.由此可知( )
第一步:H2S?H++HS- K1=
| C(H+)(HS-) |
| C(H2S) |
第二步:HS-?H++S2- K2=
| C(H+)C(S2-) |
| C(HS-) |
| A、H2S是二元弱酸 |
| B、H2S溶液中不存在HS- |
| C、0.1mol?L-1H2S溶液的pH约为4 |
| D、NaHS的电离方程式为NaHS?Na++H++S2- |
对于锌-铜-稀H2SO4组成的原电池装置中,当导线中有1mol电子通过时,理论上的电极变化是( )
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
①锌片溶解了32.5g②锌片增重32.5g③铜片上析出了1gH2④铜片上析出1mol H2⑤溶液中的SO42-移向锌极⑥溶液中SO42-移向铜极.
| A、①③⑤ | B、①④⑥ |
| C、②③⑤ | D、②④⑥ |
下列反应属于吸热反应的是( )
| A、C不完全燃烧生成CO |
| B、H2还原WO3制取W |
| C、盐酸与NaOH溶液反应 |
| D、工业上用N2与H2反应合成NH3 |
下列化学用语表述正确的是( )
A、“84消毒液”中有效成分NaCIO的电子式:Na+[
| ||||||||||||||
B、食盐中阴离子的核外电子排布式: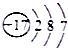 | ||||||||||||||
C、聚丙烯的结构简式: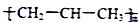 | ||||||||||||||
| D、乙烯的结构简式:CH2CH2 |
下列离子方程式的书写正确的是( )
| A、铁和稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、用小苏打治疗胃酸过多反应:CO32-+2H+═CO2↑+H2O |
| C、实验室用大理石跟盐酸反应:CO32-+2H+═CO2↑+H2O |
| D、向Ba(OH)2溶液中滴加H2SO4溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
 A、B、C、D、E、F六种物质的相互转化关系如图(反应件未标出),其中反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如图(反应件未标出),其中反应①是置换反应.