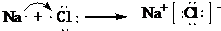
题目内容
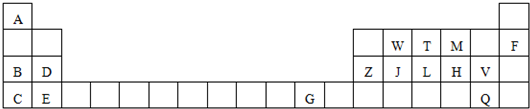
8.①②③④⑤五种元素,在元素周期表中的位置如图所示.回答下列问题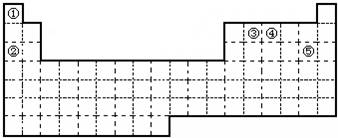
(1)①②③④⑤五种元素中,金属性最强的元素是Na(写元素名称),该元素的单质在空气中燃烧的化学方程式为2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2.
(2)元素②的最高价氧化物对应的水化物的电子式为
 ,试比较②和③原子半径的大小②>③(填“>”或“<”)
,试比较②和③原子半径的大小②>③(填“>”或“<”)(3)画出元素④的原子结构示意图
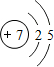 ,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)HNO3.
,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)HNO3.(4)写出元素⑤在周期表中的位置第三周期ⅦA族,以海水中含量最大的物质为原料可以生产⑤的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH.
分析 由元素在周期表中的位置可知,①为H元素、②为Na元素、③为C元素、④为N元素、⑤为Cl元素;
(1)金属性最强的元素是Na,钠在空气中加热生成过氧化钠;
(2)氢氧化钠为离子化合物,钠离子与氢氧根离子通过离子键结合而成,NaOH的电子式: ,电子层数越多半径越大;
,电子层数越多半径越大;
(3)元素氮的原子结构示意图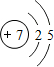 ,氮元素的最高价氧化物的水化物是硝酸能与Cu发生反应,反应中作氧化剂的是硝酸,故答案为:
,氮元素的最高价氧化物的水化物是硝酸能与Cu发生反应,反应中作氧化剂的是硝酸,故答案为: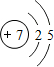 ;HNO3;
;HNO3;
(4)元素氯三个电子层,最外层7个电子,在周期表中的位置第三周期ⅦA 族,以海水中含量最大的物质为原料可以生产氯气的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH.
解答 解:由元素在周期表中的位置可知,①为H元素、②为Na元素、③为C元素、④为N元素、⑤为Cl元素;
(1)Na元素的金属性最强;钠在空气中加热生成过氧化钠,反应方程式为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,故答案为:Na;2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2;
(2)氢氧化钠为离子化合物,钠离子与氢氧根离子通过离子键结合而成,NaOH的电子式: ,电子层数越多半径越大,碳二个电子层,而钠原子三个电子层,所以②>③,故答案为:
,电子层数越多半径越大,碳二个电子层,而钠原子三个电子层,所以②>③,故答案为: ;>;
;>;
(3)元素氮的原子结构示意图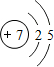 ,氮元素的最高价氧化物的水化物是硝酸能与Cu发生反应,反应中作氧化剂的是硝酸,故答案为:
,氮元素的最高价氧化物的水化物是硝酸能与Cu发生反应,反应中作氧化剂的是硝酸,故答案为: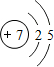 ;HNO3;
;HNO3;
(4)元素氯三个电子层,最外层7个电子,在周期表中的位置第三周期ⅦA 族,以海水中含量最大的物质为原料可以生产氯气的单质,同时还可以得到另外两种重要的工业原料,该反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH,故答案为:第三周期ⅦA 族; 2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2NaOH.
点评 本题考查元素周期表、电子式等化学用语的书写、结构与物质关系等,难度不大,注意掌握电子式的书写.

| A. | ⑧② | B. | ⑥①⑤③ | C. | ④⑤⑨ | D. | ⑦①③⑨ |
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅤⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最不活泼的元素是Ar.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
| A. | 丙烯的结构简式CH2CH2CH3 | B. | 四氯化碳的结构式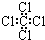 | ||
| C. | 丁烷的结构简式CH3(CH2)2CH3 | D. | 苯的分子式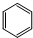 |
| A. | 手机电池在充电时,电能转变为化学能 | |
| B. | 绿色植物进行光合作用时,太阳能主要转化为化学能 | |
| C. | 煤燃烧时,化学能主要转化为热能 | |
| D. | 白炽灯工作时,电能全部转化为光能 |
 )具有多种同分异构体.
)具有多种同分异构体. ;②
;② ;③
;③ ;
;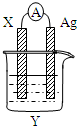 依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.
依据氧化还原反应2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.回答下列问题.