题目内容
18.X、Y、Z、W、R、M是6种短周期元素,且原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层是次外层电子数的3倍,Z、W、R、M处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.则(1)写出下列元素符号.YO RS
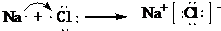
(2)已知Z单质可与M单质发生反应,反应产物是NaCl.用电子式表示该产物的形成过程:
(3)写出Z的最高价氧化物对应的水化物与W的最高价氧化物对应水化物反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
分析 X、Y、Z、W、R、M是6种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,则A为H元素;Y原子最外层电子数是次外层电子数的3倍,Y原子有2个电子层,最外层电子数为6,故Y为O元素;根据Z、W、R、M处于同一周期,R与Y处于同一族,则R为S元素;Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,则Z、W原子的核外电子数之和为8+16=24,又Z、W处于同一周期,应为第三周期,原子序数W大于Z,故Z为Na,W为Al元素,M的原子序数比S大,所以M为Cl元素,结合物质性质与元素周期律解答.
解答 解:X、Y、Z、W、R、M是6种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,则A为H元素;Y原子最外层电子数是次外层电子数的3倍,Y原子有2个电子层,最外层电子数为6,故Y为O元素;根据Z、W、R、M处于同一周期,R与Y处于同一族,则R为S元素;Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,则Z、W原子的核外电子数之和为8+16=24,又Z、W处于同一周期,应为第三周期,原子序数W大于Z,故Z为Na,W为Al元素,M的原子序数比S大,所以M为Cl元素;
(1)由分析可知,Y为O元素,R为S元素;
故答案为:O;S;
(2)已知Z单质可与M单质发生反应,反应产物是NaCl,属于离子化合物,其电子式表示的形成过程为 ;
;
故答案为:NaCl; ;
;
(3)Z的最高价氧化物对应的水化物为NaOH,W的最高价氧化物对应水化物为氢氧化铝,二者反应生成偏铝酸钠和水,则反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O;
故答案为:Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查结构与位置关系、元素周期律、微粒半径比较、离子方程式的书写等,难度中等,根据题中信息推断元素是关键,注意电子式表示物质形成过程的方法.

| A. | H2S | B. | BCl3 | C. | CO2 | D. | PCl5 |
| A. | 裂解与裂化的产物都含有不饱和烃 | |
| B. | 裂解与裂化都是烃的分解反应 | |
| C. | 裂解与裂化的原料都是石油分馏产品 | |
| D. | 裂解与裂化都是为得到气态烃 |
| A. | Na | B. | Cl | C. | F | D. | Li |
| A. | 使用适当的催化剂只改变正反应速率 | |
| B. | 降低压强能提高逆反应速率 | |
| C. | 升高温度能同时提高正、逆反应速率 | |
| D. | 减小压强对正反应速率影响小于逆反应速率的影响 |
| A. | 苯 | B. | 乙烯 | C. | 异丁烷 | D. | 新戊烷 |
| A. | 次氯酸的结构式:H-Cl-O | B. | 16O2-和18O2-的结构示意图: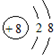 | ||
| C. | 氮气的电子式: | D. | 电子式表示氯化钠的形成过程: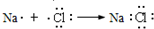 |
| A. | 14 | B. | 8 | C. | 16 | D. | 12 |
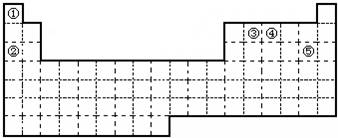
 ,试比较②和③原子半径的大小②>③(填“>”或“<”)
,试比较②和③原子半径的大小②>③(填“>”或“<”)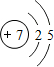 ,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)HNO3.
,该元素的最高价氧化物的水化物能与Cu发生反应,反应中作氧化剂的是(写化学式)HNO3.