题目内容
19.某1.6g有机物燃烧后的产物先通过浓H2SO4,浓H2SO4增重3.6g,后又通过碱石灰、碱石灰增重4.4g,下列说法正确的是( )| A. | 浓H2SO4增重的是CO2的质量 | B. | 该有机物中没有氧元素 | ||
| C. | 该有机物中有氧元素 | D. | 碱石灰增重的是CO2和H2O的质量 |
分析 n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,n(CO2)=$\frac{4.4g}{44g/mol}$=0.1mol,则C、H的质量和为0.2mol×2×1g/mol+0.1mol×12g/mol=1.6g,则有机物不含O元素,以此来解答.
解答 解:n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,n(CO2)=$\frac{4.4g}{44g/mol}$=0.1mol,则C、H的质量和为0.2mol×2×1g/mol+0.1mol×12g/mol=1.6g,则有机物不含O元素,
A.浓H2SO4增重的是H2O的质量,故A错误;
B.由上述分析可知,有机物不含氧元素,故B正确;
C.由上述分析可知,有机物不含氧元素,故C错误;
D.碱石灰增重的是CO2的质量,故D错误;
故选B.
点评 本题考查有机物的分子式确定的计算,为高频考点,把握水和二氧化碳的质量及原子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
10.从化学键角度分析,下列不属于化学变化的是( )
| A. | 金刚石变为石墨 | B. | 蔗糖溶解 | ||
| C. | CuSO4吸水生成结晶水合物 | D. | NH3溶于水 |
7.下列说法不正确的是( )
| A. | 常温下,醋酸钠与醋酸的混合溶液pH=7,c(Na+)=c(CH3COO-) | |
| B. | 常温下,将pH=1的醋酸溶液稀释100倍后,水电离的c(H+)=10-11mol/L | |
| C. | 0.1 mol/L Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| D. | 0.1mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
4.下列化合物中,不能由单质直接化合而得到的是( )
| A. | FeCl2 | B. | Na2O2 | C. | FeS | D. | Fe3O4 |
11.下列各反应,生成物不随反应条件或反应物的用量变化而变化的是( )
| A. | NaHCO3和盐酸 | B. | Ca(OH)2和CO2 | C. | Na和O2 | D. | AlCl3与NaOH |
 .
. HN3+OH-.
HN3+OH-. ,
, ;
;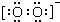 ;
; .
.