题目内容
1.完成下列各题:(1)铜与浓硝酸可发生反应:Cu+4HNO3(浓)═Cu(NO3)2 +2NO2↑+2H2O,其中铜被氧化 (填“氧化”或“还原”),浓硝酸作氧化 (填“氧化”或“还原”)剂.在该反应中,若消耗了1mol Cu,则生成2 mol NO2
(2)3.01×1023个氯气分子的物质的量是0.5mol;1.5 mol Na2SO4•10H2O中所含的Na+的物质的量是3mol,所含的SO42-的物质的量是1.5mol,所含H2O的数目是15NA
(3)4种物质:①NH3、②SO2、③NaCl溶液、④H2SO4溶液.其中,能使品红溶液褪色的是② (填序号,下同),焰色反应呈黄色的是,遇氯化氢有白烟产生的是①,与氯化钡溶液反应产生白色沉淀的是④
(4)某些铁、铝制品的表面常生成一层氧化物,其主要成分分别是氧化铁、氧化铝.请回答:
a.两种氧化物均能与盐酸反应,生成的两种盐的化学式分别为FeCl3、AlCl3.向这两种盐的溶液中分别滴加足量氢氧化钠溶液,可观察到:其中一种溶液中的现象是先产生白色沉淀,然后白色沉淀逐渐消失;另一种溶液中的现象是②(填序号).
①产生白色沉淀
②产生红褐色沉淀
③产生白色沉淀,迅速变成灰绿色,最后变成红褐色
b.铝与氧化铁的反应可用于焊接钢轨,其反应的化学方程式为2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
分析 (1)该反应中,铜元素化合价由0价变为+2价、N元素化合价由+5价变为+4价,失电子化合价升高的反应物被氧化,得电子化合价降低的反应物是氧化剂,根据铜和二氧化氮之间的关系式计算;
(2)3.01×1023个氯气分子的物质的量是$\frac{3.01×10{\;}^{23}}{6.02×10{\;}^{23}mol{\;}^{-1}}$=0.5mol;根据n(Na+)=2n(Na2SO4•10H2O)=2n(SO42-)、n(H2O)=10n(Na2SO4•10H2O)解答;
(3)SO2能够使品红溶液褪色,加热后又会恢复原色;焰色反应呈现黄色的是Na元素;NH3容易挥发,遇到氯化氢,生成氯化铵小颗粒,有白烟产生;四种物质中能够和氯化钡反应生成沉淀的是H2SO4;
(4)a、氧化铁和氧化铝分别和盐酸反应生成盐和水,向氯化铁溶液中滴加氢氧化钠,氢氧化钠和氯化铁溶液反应生成红褐色氢氧化铁沉淀;
b、铝和氧化铁发生铝热反应且放出大量热,从而用于焊接钢轨,根据反应物、生成物及反应条件书写方程式.
解答 解:(1)该反应中,铜元素化合价由0价变为+2价、N元素化合价由+5价变为+4价,所以硝酸是氧化剂、Cu是还原剂,还原剂被氧化,所以Cu被氧化,在该反应中,根据Cu和二氧化氮之间的关系式知,若消耗了1mol Cu,则生成2mol NO2,
故答案为:氧化;氧化;2;
(2)3.01×1023个氯气分子的物质的量是$\frac{3.01×10{\;}^{23}}{6.02×10{\;}^{23}mol{\;}^{-1}}$=0.5mol;Na2SO4•10H2O在水中电离方程式为:Na2SO4•10H2O=2Na++SO42-+10H2O,所以Na2SO4•10H2O中n(Na+)=2n(Na2SO4•10H2O)=2n(SO42-),则1.5mol Na2SO4•10H2O中所含的Na+的物质的量是3mol;所含的SO42-的物质的量是1.5mol;所含H2O的数目N(H2O)=10n(Na2SO4•10H2O)×NA=15NA,
故答案为:0.5mol;3mol;1.5mol;15;
(3)SO2能够使品红溶液褪色,加热后又会恢复原色,故能使品红溶液褪色的是②;
钠元素焰色反应呈现黄色,所以焰色反应呈黄色的是③;
NH3 易挥发,遇到氯化氢后会生成氯化铵小颗粒,产生白烟现象,故遇氯化氢有白烟产生的是①;
四种物质中能够和氯化钡反应生成沉淀的是H2SO4,故四种物质中能够和氯化钡反应生成沉淀的是④,
故答案为:②;③;①;④;
(4)a、氧化铁和盐酸反应方程式为Fe2O3+6HCl=2FeCl3+3H2O,氧化铝和盐酸反应方程式为:Al2O3+6HCl=2AlCl3+3H2O,所以二者得到的盐分别是FeCl3、AlCl3,向AlCl3溶液中滴加氢氧化钠,现象是先产生白色沉淀,然后白色沉淀逐渐消失;向氯化铁溶液中滴加氢氧化钠,氢氧化钠和氯化铁溶液反应,立即生成红褐色氢氧化铁沉淀,所以看到的现象是产生红褐色沉淀,故选②,
故答案为:FeCl3;AlCl3;②;
b、铝和氧化铁发生铝热反应且放出大量热,从而用于焊接钢轨,反应方程式为:2Al+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,故答案为:2Al+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
点评 本题考查了氧化还原反应、有关物质的量的计算以及元素化合物的相关性质,明确物质的性质是解本题关键,根据物质的性质来分析解答,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 试管 | B. | 量筒 | C. | 烧杯 | D. | 圆底烧瓶 |
| A. | 铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ | |
| B. | 大理石与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ | |
| D. | 氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
| A. | 2:3 | B. | 3:2 | C. | l:1 | D. | l:6 |
| A. | N2O | B. | N2O3 | C. | NO2 | D. | N2O4 |
利用这一反应,下列所给化合物中可以与钠反应合成环丁烷的是( )
①CH3Br ②CH2BrCH2CH2CH2Br ③CH2BrCH2Br ④CH3CH2CH2CH2Br ⑤CH3CH2BrCHCH2Br.
| A. | ①③⑤ | B. | ①④⑤ | C. | ②③ | D. | ①②③④⑤ |
| A. | 2H2(g)+O2(g)═2H2O(g)△H1 2H2(g)+O2(g)═2H2O(l)△H2 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | 2HCl(g)═H2(g)+Cl2(g)△H1 H2(g)+Cl2(g)═2HCl(g)△H2 |
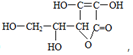 其分子式为C6H8O6,也称为抗坏血酸.碘和铁是人体必需的微量元素,我国采用食盐补碘(具体为KIO3)、酱油补铁.
其分子式为C6H8O6,也称为抗坏血酸.碘和铁是人体必需的微量元素,我国采用食盐补碘(具体为KIO3)、酱油补铁.