题目内容
16.下列离子方程式中,正确的是( )| A. | 铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ | |
| B. | 大理石与稀盐酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ | |
| D. | 氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
分析 A.离子方程式两边正电荷不相等,违反了电荷守恒;
B.大理石的主要成分为碳酸钙,碳酸钙不能拆开;
C.铜不与稀硫酸反应;
D.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水.
解答 解:A.铁与氯化铁溶液反应生成氯化亚铁,正确的离子方程式为:Fe+2Fe3+=3Fe2+,故A错误;
B.大理石与稀盐酸反应,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故B错误;
C.Cu的活泼性较弱,不与稀硫酸反应,无法书写离子方程式,故C错误;
D.氯气与氢氧化钠溶液反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
6.下列气体可用向上排空气法收集的是( )
| A. | NH3 | B. | H2 | C. | Cl2 | D. | CH4 |
7.通常情况下,不能用铁制容器盛放的是( )
| A. | 浓硫酸 | B. | 盐酸 | C. | 汽油 | D. | 酒精 |
4.在一定的条件下,氯酸钾和碘可发生反应:2KClO3+I2═2KIO3+Cl2,由此可推断下列相应的结论中,错误的是( )
| A. | 该反应属于置换反应 | B. | 还原性:I2>Cl2 | ||
| C. | 氧化性:KClO3>KIO3 | D. | I2 是氧化剂 |
8.己知有如下反应:①2BrO3-+Cl2═Br2+2ClO3-
②ClO-+5Cl-+6H+═3Cl2+3H2O
③2FeCl2+Cl2═2FeCl3
根据上述反应,判断下列结论中错误的是( )
②ClO-+5Cl-+6H+═3Cl2+3H2O
③2FeCl2+Cl2═2FeCl3
根据上述反应,判断下列结论中错误的是( )
| A. | Cl2是在反应②中既是氧化产物又是还原产物 | |
| B. | 氧化性强弱的顺序为:BrO3->ClO3->Cl2>Fe3+ | |
| C. | 溶液中可发生:ClO3-+6Fe2++6H+═Cl-+6Fe3++3H2O | |
| D. | Cl2在①、③反应中均作氧化剂 |
5.表是A、B、C、D五中有机物质的相关信息:
(1)A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(2)A与溴的四氯化碳溶液反应的生成物的结构简式CH2BrCH2Br;该生成物在一定条件下可用于制取最简单的二元醇方程式为:CH2BrCH2Br+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaBr.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在催化剂作用下,B与溴反应的化学方程式: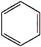 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.
(4)C与E反应能生成酯,该反应类型为取代反应;其化学反应方程式为:CH2=CHCOOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH2=CHCOOOCH2CH3+H2O.
(5)D在一定条件下能发生银镜反应,其化学反应方程式:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
| A | B | C | D | E |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与水在一定条件下反应生成C | ①由C、H两种元素组成; ②球棍模型为  | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. | ①相对分子质量比C少2; ②能由C氧化而成; | ①由C、H、O三种元素组成; ②球棍模型为:  |
(2)A与溴的四氯化碳溶液反应的生成物的结构简式CH2BrCH2Br;该生成物在一定条件下可用于制取最简单的二元醇方程式为:CH2BrCH2Br+2NaOH$→_{△}^{水}$CH2OHCH2OH+2NaBr.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在催化剂作用下,B与溴反应的化学方程式:
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.(4)C与E反应能生成酯,该反应类型为取代反应;其化学反应方程式为:CH2=CHCOOH+CH3CH2OH$?_{△}^{H_{2}SO_{4}}$CH2=CHCOOOCH2CH3+H2O.
(5)D在一定条件下能发生银镜反应,其化学反应方程式:CH3CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
6.下列说法中正确的是( )
| A. | 元素从化合态变为游离态,该元素一定被还原 | |
| B. | 铝合金比纯铝的熔点更高 | |
| C. | 保存FeCl3溶液时,通常在溶液中加少量的单质铁 | |
| D. | 漂白粉应隔绝空气密封保存 |