题目内容
12.下列表示对应化学反应的离子方程式正确的是( )| A. | 用Na与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 少量Ca(HCO3)2溶液与NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 石灰石溶于稀盐酸:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 铁与硫酸铜溶液反应:2Fe+3Cu2+═2Fe3++3Cu |
分析 A.原子个数不守恒;
B.二者反应生成碳酸钙、碳酸钠和水;
C.二者反应生成氯化钙、二氧化碳和水;
D.不符合反应客观事实.
解答 解:A.用Na与水反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.少量Ca(HCO3)2溶液与NaOH溶液反应,离子方程式:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故B错误;
C.石灰石溶于稀盐酸,离子方程式:CaCO3+2H+═Ca2++H2O+CO2↑,故C正确;
D.铁与硫酸铜溶液反应生成硫酸亚铁和铜,离子方程式:Fe+Cu2+═Fe2++Cu,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
2.下列实验装置能达到实验目的是( )
| A. | 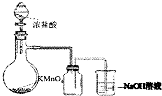 实验室制取并收集Cl2 | B. | 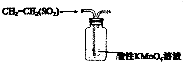 检验乙烯中是否含有SO2 | ||
| C. | 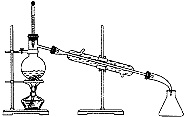 分离Br2和H20的混合物 | D. | 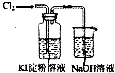 验证氧化性Cl>I2 |
3.氢化钠可以作为生氢剂(其中NaH中氢元素为-1价),反应方程式如下:NaH+H2O═NaOH+H2↑,则下列说法正确的是( )
| A. | 反应是置换反应,反应中有2个电子转移 | |
| B. | 反应是复分解反应 | |
| C. | 反应是氧化还原反应,反应中电子转移数为1 | |
| D. | 反应的离子方程式为H-+H+═H2↑ |
7.下列有关氧化还原反应的说法正确的是( )
| A. | 一定有电子得失或偏移 | B. | 氧化反应一定先于还原反应 | ||
| C. | 氧化剂发生氧化反应 | D. | 其实质是元素化合价发生变化 |
2.下列说法正确的是( )
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的质量数不同,属于两种元素 | |
| B. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、H2互为同位素 | |
| C. | 14462Sm其原子核内中子数和质子数都是62 | |
| D. | O2和O3互为同素异形体 |
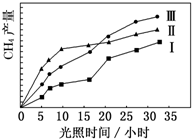 利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.
利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.