��Ŀ����
1����1��8g CH4����2mol��ԭ�ӣ�0.1mol NH3����Լ0.4NA��ԭ�ӣ�ͬ��ͬѹ�£�ͬ�����NH3��H2S�����������Ϊ1��2��ͬ��ͬѹ�£�ͬ������NH3��H2S����������Ϊ2��1����2���ڱ�״���£�15gij����ķ�������11.2L CO�ķ�������ȣ���������Ħ������Ϊ30g/mol��
��3��V L Fe2��SO4��3��Һ�к�Fe3+m g�������Һ��Fe3+�����ʵ���Ũ��Ϊ$\frac{m}{56V}$ mol•L-1�����ʵ����ʵ���Ũ��Ϊ$\frac{m}{112V}$ mol•L-1��
��4������֬�ް�סԼ0.2g�������Ʒ�δ������ʯ�����ϣ�����֬���ϵμ���ˮ���ɹ۲쵽��֬��ȼ����������ʵ���������ó����йع������ƺ�ˮ��Ӧ�Ľ����ǣ�a�����������ɣ�b��Na2O2��ˮ��Ӧ�Ļ�ѧ����ʽ��2Na2O2+2H2O=4NaOH+O2����
���� ��1��1molCH4�к���4mol����ԭ�ӣ�����N=nNA��ͬ��ͬѹ�£�ͬ�����NH3��H2S�������ʵ�����ȣ�����m=nM���м�����⣻����n=$\frac{m}{M}$������⣻
��2������n=$\frac{m}{M}$����CO���ʵ�����15��������CO������Ŀ��ȣ���������ʵ�����ȣ��ٸ���M=$\frac{m}{n}$���������Ħ��������
��3������n=$\frac{m}{M}$����m gFe3+�����ʵ������ٸ���c=$\frac{n}{V}$�������Һ��Fe3+�����ʵ���Ũ�ȣ���Fe3+�غ��֪��c[Fe2��SO4��3]=$\frac{1}{2}$c��Fe3+����
��4��ȼ�յ������ǣ������ʾ��п�ȼ�ԣ��ڿ�ȼ���������Ӵ������¶ȴﵽ��ȼ����Ż�㣬����ȼ��ȼ�յ������������������ƺ�ˮ��Ӧ�����������ƺ�������
��� �⣺��1��1molCH4�к���4mol����ԭ�ӣ�8g CH4�����ʵ���Ϊ��$\frac{8g}{16g/mol}$=0.5mol��������ԭ�ӵ����ʵ�����0.5��4=2mol������N=nNA=0.1��4NA=0.4NA��ͬ��ͬѹ�£�ͬ�����NH3��H2S�������ʵ�����ȣ���������֮��Ϊ��17��34=1��2�����֮�ȵ������ʵ���֮�ȣ�$\frac{1}{17}��\frac{1}{34}$=2��1���ʴ�Ϊ��2��0.4NA��1��2��2��1��
��2��11.2L CO�����ʵ���=$\frac{11.2L}{22.4L/mol}$=0.5mol��15��������CO������Ŀ��ȣ���������ʵ�����ȣ��ʸ�����Ħ������=$\frac{15g}{0.5mol}$=30g/mol��
�ʴ�Ϊ��30g/mol��
��3��m gFe3+�����ʵ���Ϊ$\frac{mg}{56g/mol}$=$\frac{m}{56}$mol�������Һ��Fe3+�����ʵ���Ũ��Ϊ$\frac{\frac{m}{56}}{V}$=$\frac{m}{56V}$mol/L��
��Fe3+�غ��֪��c[Fe2��SO4��3]=$\frac{1}{2}$c��Fe3+��=$\frac{1}{2}$��$\frac{m}{56V}$mol/L=$\frac{m}{112V}$mol/L��
�ʴ�Ϊ��$\frac{m}{56V}$��$\frac{m}{112V}$��
��4����֬��ȼ����Ҫ���������¶ȴﵽ�Ż�㣬˵������������ˮ��Ӧ�����������ɣ�ͬʱ�����������ȣ��÷�ӦΪ���ȷ�Ӧ���������ƺ�ˮ��Ӧ�����������ƺ�����������ʽΪ2Na2O2+2H2O=4NaOH+O2�����ʴ�Ϊ���÷�Ӧ�Ƿ��ȷ�Ӧ��2Na2O2+2H2O=4NaOH+O2����
���� ���⿼�����ʵ���Ũ�ȵ��йؼ��㣬�Ƚϻ�����ע��Թ�ʽ������������ã�ע������Ũ������Ӧ����Ũ�ȵĹ�ϵ��

 ��У����ϵ�д�
��У����ϵ�д�| A�� | ��Һ�������� | B�� | �ܼ����������仯 | ||
| C�� | ��ҺΪ������Һ��Ũ�Ȳ��� | D�� | �о����������ܼ��������� |
| A�� | ��Na��ˮ��Ӧ��Na+H2O�TNa++OH-+H2�� | |
| B�� | ����Ca��HCO3��2��Һ��NaOH��Һ��Ӧ��Ca2++HCO3-+OH-�TCaCO3��+H2O | |
| C�� | ʯ��ʯ����ϡ���CaCO3+2H+�TCa2++H2O+CO2�� | |
| D�� | ��������ͭ��Һ��Ӧ��2Fe+3Cu2+�T2Fe3++3Cu |
��1��NOx������β���е���Ҫ��Ⱦ��֮һ��
��NOx���γ����꣬��NO2�γɵ������к��е���Ҫ������H+��NO3-��
����������������ʱ�ĸ��»�����N2��O2��Ӧ����Ӧ�Ļ�ѧ����ʽ��N2+O2�T2NO��
��2��Ϊ����SO2���ŷţ�����ȡһЩ��Ч��ʩ��
���ں���ú�м�����ʯ�ҿ�����������ã�ȼ�չ����У���Ԫ��ת���������̬�Ļ�����û�����Ļ�ѧʽ��CaSO4��
�����������У����������������е�SO2����ad������ţ���
a��Na2CO3 b��H2SO4 c��NaHSO3 d��NH3•H2O
��3��ȡij��������������ˮ�����Ƴɴ���Һ���������������Ӽ���Ũ�������
| ���� | K+ | Na+ | NH4+ | H+ | SO42- | NO3- | Cl- |
| Ũ��/mol•L-1 | 4��10-6 | 6��10-6 | 2��10-5 | a | 4��10-5 | 3��10-5 | 2��10-5 |
| A�� | ��ɫ | B�� | ��ɺ�ɫ | C�� | ����ɫ���� | D�� | �ȱ�����ɫ |
| A�� | ����������Һ��ͨ��SO2��Ca2++2ClO-+H2O+SO2�TCaSO3��+2HClO | |
| B�� | ����������Һ�еμ���������ֱ�������������3Ba2++6OH-+2Al3++3SO42-�T3BaSO4��+2Al��OH��3�� | |
| C�� | ���⻯�Ʒ������룺HS-+H2O�TH3O++S2- | |
| D�� | ��ʳ���������е�Ħ����̼��ƣ�CaCO3+2H+�TCa2++H2O+CO2�� |
| A�� | 0.1mol/LNa2S2O3��H2SO4��5mL����ˮ5mL����Ӧ�¶�10�� | |
| B�� | 0.1mol/LNa2S2O3��H2SO4��5mL����ˮ10mL����Ӧ�¶�10�� | |
| C�� | 0.1mol/LNa2S2O3��H2SO4��5mL����ˮ5mL����Ӧ�¶�30�� | |
| D�� | 0.2mol/LNa2S2O3��H2SO4��5mL����ˮ10mL����Ӧ�¶�30�� |
| A�� | ��״���£�22.4 L CCl4�ķ�����ԼΪNA�� | |
| B�� | ���³�ѹ�£�3.2gO2��O3��������к��е���ԭ����ĿΪ0.2NA | |
| C�� | ��״���£�0.1molCl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA | |
| D�� | ���¸�ѹ�£�28gN2��6gH2��Ӧ�����ɵ�NH3������Ϊ2nA |
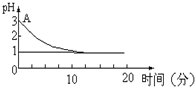 ���ڡ�����Ȼ�ͭ��Һʱ��pHֵ�仯�����⣬��ѧ�����������ֲ�ͬ�Ĺ۵㣺
���ڡ�����Ȼ�ͭ��Һʱ��pHֵ�仯�����⣬��ѧ�����������ֲ�ͬ�Ĺ۵㣺