题目内容
20.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )| A. | 44g二氧化碳气体中含有共用电子对数目为2NA | |
| B. | 室温下,1L0.1 mol•L-1的Na2CO3溶液中,CO32-离子数目为0.1NA | |
| C. | 6.0g碳在8.4L氧气(标准状况)中燃烧,转移的电子数为1.5NA | |
| D. | 500mL1.0mol•L-1盐酸与0.435gMnO2共热后,生成Cl2分子的数目为0.005NA |
分析 A、求出二氧化碳的物质的量,然后根据二氧化碳中含4对共用电子对来分析;
B、碳酸根在溶液中会水解;
C、6g碳的物质的量为0.5mol,而标况下8.4L氧气的物质的量为0.375mol,故氧气不足,根据氧气反应后变为-2价来分析;
D、二氧化锰只能和浓盐酸反应,和稀盐酸不反应.
解答 解:A、44g二氧化碳的物质的量为1mol,而二氧化碳中含4对共用电子对,故1mol二氧化碳中共含4NA对共用电子对,故A错误;
B、碳酸根在溶液中会水解,故溶液中的碳酸根的个数小于0.1NA个,故B错误;
C、6g碳的物质的量为0.5mol,而标况下8.4L氧气的物质的量为0.375mol,故氧气不足,而氧气反应后变为-2价,故0.375mol氧气转移1.5NA个电子,故C正确;
D、二氧化锰只能和浓盐酸反应,和稀盐酸不反应,故浓盐酸不能反应完全,则生成的氯气的分子个数小于0.005NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
10.已知阿伏伽德罗常数可表示为NA,则下列说法正确的是( )
| A. | 17gNH3所含中子数目为10 NA | |
| B. | 常温常压下,22 g氧气和26 g臭氧所含的氧原子总数为3NA | |
| C. | 常温常压下,18g H2O含有的电子总数为8NA | |
| D. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
11.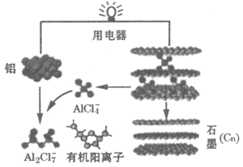 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
 2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )
2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4-和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( )| A. | 放电时,铝为负极、石墨为正极 | |
| B. | 放电时,有机阳离子向铝电极方向移动 | |
| C. | 放电时的负极反应为:Al-3e-+7AlCl4-═4Al2Cl7- | |
| D. | 充电时,AlCl4-向石墨电极方向移动 |
15.下列关于铁及其化合物的说法不正确的是( )
| A. | 炼铁原料有铁矿石、焦炭、空气和石灰石 | |
| B. | FeCl3溶液能使KI淀粉溶液变蓝色 | |
| C. | 灼热的铁丝放入盛有干燥氯气的集气瓶中燃烧生成棕色的烟雾 | |
| D. | 利用Cu与FeCl3溶液的反应制作印刷电路板 |
5.食品添加剂可以改善食品感官,增强食欲.下列添加剂中不属于调味剂的是( )
| A. | 食盐 | B. | 味精 | C. | 小苏打 | D. | 食醋 |
4.已知H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)↓+2H2O(l)△H=-1 584.2kJ•mol-1;HCl(aq)与NaOH(aq)反应的中和热△H=-55.6kJ•mol-1.则生成SO42-(aq)+Ba2+(aq)=BaSO4(s)的反应热等于( )
| A. | -1 528.6 kJ•mol-1 | B. | -1 473 kJ•mol-1 | ||
| C. | +1 473 kJ•mol-1 | D. | +1 528.6 kJ•mol-1 |
5.只能表示一个化学反应的离子方程式是( )
| A. | Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | CO32-+2H+=H2O+CO2↑ | |
| C. | 2Br-+Cl2=2Cl-+Br2 | |
| D. | SO2+Cl2+2H2O=4H++2Cl-+SO42- |