题目内容
8.下列各物质的转化关系如下图所示.B、D是气体,其中B是空气的主要成分之一;C是淡黄色固体,常用于供氧剂;E是红棕色固体;F是最常见的无色液体.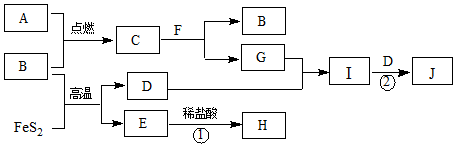
回答下列问题:
(1)C的化学式是Na2O2.
(2)气体D通入紫色石蕊溶液的现象是石蕊溶液变红.
(3)写出反应①的离子方程式Fe2O3+6H+=2Fe3++3H2O.
(4)写出反应②的化学方程式Na2SO3+SO2+H2O=2NaHSO3.
分析 B是空气的主要成分之一,可与FeS2反应,应为O2,则D为SO2,C是淡黄色固体,常用于供氧剂,为Na2O2,则A为Na,F是最常见的无色液体,应为H2O,由转化关系可知G为NaOH,I为Na2SO3,J为NaHSO3,E是红棕色固体,应为Fe2O3,则H为FeCl3,结合对应物质的性质以及题目要求解答该题.
解答 解:(1)由以上分析可知C为Na2O2,故答案为:Na2O2;
(2)D为SO2,为酸性气体,可使石蕊溶液变红,故答案为:石蕊溶液变红;
(3)反应①的离子方程式为Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;
(4)反应②的化学方程式为Na2SO3+SO2+H2O=2NaHSO3,故答案为:Na2SO3+SO2+H2O=2NaHSO3.
点评 本题考查无机物推断,为高频考点,侧重考查学生的分析能力,题目难度中等,涉及Na、S元素单质及其化合物性质,“B是空气的主要成分之一;C是淡黄色固体,常用于供氧剂;E是红棕色固体;F是最常见的无色液体”为推断突破口,侧重分析与推断能力的综合考查.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
7.近日由美国斯坦福大学研究团队利用微加工技术在二氧化硅薄片上蚀刻微米量级的小孔,设计出一种能为太阳能电池板降温的二氧化硅光子晶体涂层材料.下列关于该材料的说法正确的是( )
| A. | 该材料耐高温、易导热、耐酸碱性强 | |
| B. | 该材料的主要成分也可用于制作太阳能电池板 | |
| C. | 网络通讯所用的光导纤维与该材料具有相同的化学成分 | |
| D. | 该光子晶体是平面网状结构,每隔Si与2个O成键,每个O与2个Si成键 |
19.下列物质的导电性能最差的是( )
| A. | 熔化的氢氧化钠 | B. | 0.1 mol/L盐酸 | C. | 0.1 mol/L醋酸 | D. | 氯化钾固体 |
3.关于NaHCO3和Na2CO3的性质判断正确的是( )
| A. | 常温下溶解度:NaHCO3>Na2CO3 | |
| B. | 常温下,相同物质的量浓度溶液的碱性:NaHCO3>Na2CO3 | |
| C. | 热稳定性:NaHCO3<Na2CO3 | |
| D. | 与同浓度、同体积的盐酸反应生成气体的快慢:NaHCO3<Na2CO3 |
13.下列物质的水溶液因水解而呈酸性的是( )
| A. | CH3COOH | B. | (NH4)2Fe (SO4)2 | C. | NaHCO3 | D. | NaHSO4 |
20.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 44g二氧化碳气体中含有共用电子对数目为2NA | |
| B. | 室温下,1L0.1 mol•L-1的Na2CO3溶液中,CO32-离子数目为0.1NA | |
| C. | 6.0g碳在8.4L氧气(标准状况)中燃烧,转移的电子数为1.5NA | |
| D. | 500mL1.0mol•L-1盐酸与0.435gMnO2共热后,生成Cl2分子的数目为0.005NA |
17.136C-NMB(核磁共振)可用于含碳化合物的结构分析,下列关于136C说法正确的是( )
| A. | 核外有13个电子,核内有13个质子 | |
| B. | 质量数为13,原子序数为6,核内有7个质子 | |
| C. | 136C与126C互为同位素 | |
| D. | 质量数为13,质子数为6,中子数为6 |
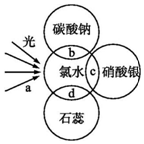 氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)
氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)