题目内容
【题目】元素的以下性质,随着原子序数的递增不呈周期性变化的是( )
A.化合价B.原子半径
C.元素的失电子性和得电子性D.相对原子质量
【答案】D
【解析】
A.同一周期从左到右,最高正价:+1→+7,最低负价-4→-1,同一主族,最高正价相同,最低负价相同(除F、O外),故A错误;
B.原子半径同一周期从左到右逐渐减小(稀有气体最大),同一主族从上到下逐渐增大,故B错误;
C.得失电子能力同一周期从左到右失电子能力减弱,得电子能力增强,同一主族从上到下失电子能力增强,得电子能力减弱,故C错误;
D.相对原子质量不随原子序数递增而呈现周期性变化,故D正确;
综上所述,答案为D。

【题目】(1)固体可分为晶体、非晶体和准晶体三大类,可通过________________方法区分晶体、非晶体和准晶体,以色列科学家丹尼尔·谢赫特曼因发现锰的化合物准晶体而独享了2011年诺贝尔化学奖。基态Mn原子的电子排布式为_______________。
(2)PCl3的立体构型为______________,中心原子的杂化轨道类型_______________。
(3)硼的卤化物在工业中有重要作用,硼的四种卤化物的沸点如下表所示。
BF3 | BCl3 | BBr3 | BI3 | |
沸点/K | 172 | 285 | 364 | 483 |
①四种卤化物沸点依次升高的原因是___________________。
②B、C、N、O三种元素第一电离能由小到大的顺序为___________。
③用BF3分子结构解释反应BF3(g)+NH4F(s)=NH4BF4(s)能够发生的原因:____________。
(4)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
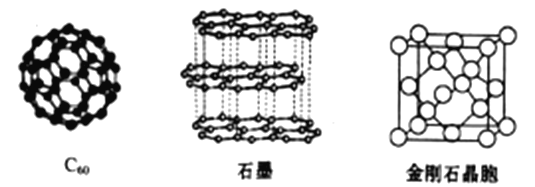
回答下列问题
①石墨晶体中,层内C-C键的键长为142pm,而金刚石中C-C键的键长为154pm,其原因是金刚石中只存在C-C间的________共价键,而石墨层内的C-C间存在_________键。
②金刚石晶胞含有___________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,列式表示碳原子在晶胞中的空间占有率__________(不要求计算结果)。