题目内容
【题目】下图所示的实验操作与方法正确的是( )
A.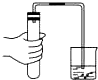 检验装置气密性
检验装置气密性
B.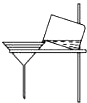 过滤
过滤
C.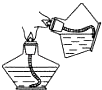 点燃酒精灯
点燃酒精灯
D.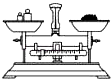 称量氯化钠
称量氯化钠
【答案】A
【解析】解:A.在检验装置的气密性时,利用的是装置内气体的压强改变,有气泡冒出时,说明装置气密性良好,否则气密性不好,故A正确;
B.过滤实验中要用玻璃棒引流,图中没有,故B错误;
C.点燃酒精灯时,用火柴点燃,如果用燃着的酒精灯去点燃另一个酒精灯,会引起酒精失火,造成危险.图中操作错误,故C错误;
D.托盘天平的使用要注意“左物右码”的原则,图中正好相反,故D错误.
故选A.
A.在检查装置的气密性时,先将导管放入水槽中,然后用手握住试管外壁;
B.过滤实验中要用玻璃棒引流;
C.点燃酒精灯时,不能用燃着的酒精灯去点燃另一个酒精灯;
D.托盘天平的使用要注意“左物右码”的原则.

【题目】用软锰矿[主要成分MnO2,还含Fe2O3、Cu2(OH)2CO3及少量不溶于水和酸的杂质]和酸洗厂废酸液(含1mol/LH2SO4的FeSO4溶液)联合生产硫酸锰和铁红(Fe2O3),生产过程如下图:

Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.3 | 6.3 | 4.7 | 2.7 |
完全沉淀时 | 9.8 | 8.3 | 6.7 | 3.6 |
(1)过程①~④所涉及的实验操作方法中,包含过滤的有______(写序号)。
(2)溶液1中,先通入O2,其作用是_______。
(3)由固体2得到铁红的化学方程式是_______。
(4)下列说法正确的是______(填字母)。
a.过程①中有氧化还原反应发生
b.加入MnS的目的是除去溶液中的Cu2+,增大Mn2+
c.溶液1中含有的阳离子主要是Fe2+、Fe3+、Cu2+、Mn2+、H+
【题目】一个原电池的总反应的离子方程式是Zn+Cu2+====Zn2++Cu,该反应的原电池的正确组成是( )
正极 | 负极 | 电解质溶液 | |
A. | Zn | Cu | CuCl2 |
B. | Cu | Zn | CuSO4 |
C. | Zn | Cu | ZnCl2 |
D. | Cu | Zn | ZnSO4 |
A. A B. B C. C D. D