题目内容
18.“绿色化学”特点之一是:提高原子的利用率,力图使所有作为原料的原子都被产品所消纳,实现“零排放”.以下反应不符合绿色化学原子经济性要求的是( )| A. | 乙烯在银作催化剂的条件下与氧气反应生成环氧乙烷 | |
| B. | 乙烯水化法制乙醇 | |
| C. | 乙烯与氯化氢加成制氯乙烷 | |
| D. | 利用乙烯与氢气加成制得的乙烷与氯气在光照条件下制氯乙烷 |
分析 反应符合绿色化学原子经济性要求,则反应物必须全部转化为生成物,可为加成反应,且没有气体副产品生成,以此解答该题.
解答 解:A.乙烯与氧气在银的催化作用下生成环氧乙烷,反应物全部转化为环氧乙烷从理论、经济、环保及操作等方面都很好,符合绿色化学思想,故A不选;
B.乙烯与水制备乙醇,产物只有一种,为加成反应,原料利用率为100%,故B不选;
C.乙烯与氯化氢加成制氯乙烷,产物只有一种,为加成反应,原料利用率为100%,故C不选;
D.乙烷与氯气制备一氯乙烷为取代反应,有副产品HCl、二氯乙烷、三氯乙烷等生成,故D选.
故选D.
点评 本题考查有机物的结构和性质,侧重于化学与生活、生产的考查,有利于培养学生良好的科学素养,提高学习的积极性,题目涉及绿色化学,明确实质是反应物全部反应生成所需的产物,不造成浪费、污染,根据题目信息解答.

练习册系列答案
相关题目
8.取a g某物质在氧气中完全燃烧,将其全部产物跟足量的过氧化钠固体完全反应,反应后固体的质量恰好也增加了a g.下列物质中能满足上述结果的是( )
①H2
②CO
③CH4
④C6H12O6
⑤HCOOH
⑥C12H22O11.
①H2
②CO
③CH4
④C6H12O6
⑤HCOOH
⑥C12H22O11.
| A. | ③⑥ | B. | 只有①② | C. | ①②④ | D. | 只有 ⑤ |
9.钴(Co)及其化合物在工业上有广泛应用.为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质).
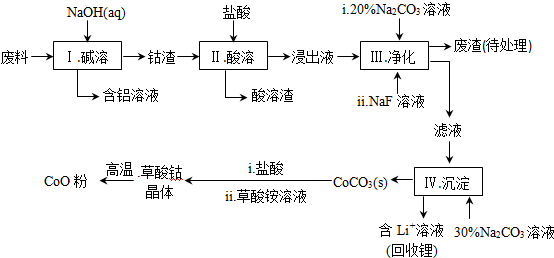
已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)写出步骤Ⅱ中Co2O3与盐酸反应生成氯气的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O;
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过7.15,废渣中的成分有LiF、Fe(OH)3;
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀;
(5)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二元化合物,该化合物中钴元素的质量分数为73.44%.此过程发生反应的化学方程式是3CoC2O4+2O2$\frac{\underline{\;210-290℃\;}}{\;}$Co3O4+6CO2;
(6)某锂离子电池的总反应为C+LiCoO2 LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)写出步骤Ⅱ中Co2O3与盐酸反应生成氯气的离子方程式Co2O3+6H++2Cl-=2Co2++Cl2↑+3H2O;
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过7.15,废渣中的成分有LiF、Fe(OH)3;
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是降低溶液中Li+浓度,避免步骤Ⅳ中产生Li2CO3沉淀;
(5)在空气中加热CoC2O4固体,经测定,210~290℃的过程中只产生CO2和一种二元化合物,该化合物中钴元素的质量分数为73.44%.此过程发生反应的化学方程式是3CoC2O4+2O2$\frac{\underline{\;210-290℃\;}}{\;}$Co3O4+6CO2;
(6)某锂离子电池的总反应为C+LiCoO2
 LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
LixC+Li1-xCoO2,LixC中Li的化合价为0价,该锂离子电池充电时阳极的电极反应式为LiCoO2-xe-=Li1-xCoO2+xLi+.
6.有关实验的说法中正确的是( )
| A. | 除去铁粉中的铜粉,加入足量浓硫酸加热反应后进行过滤 | |
| B. | 不用任何其他试剂就可以鉴别NaOH溶液和Al2(SO4)3溶液 | |
| C. | 制备Fe(OH)3胶体时,通常是将Fe(OH)3固体溶于沸水中 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
3.下列物质中,不能使高锰酸钾酸性溶液褪色的是( )
| A. | 乙炔 | B. | 甲苯 | C. | 苯 | D. | 乙烯 |
10.下列有关钠及其化合物的说法不正确的是( )
| A. | 电解饱和食盐水不可制取金属钠 | |
| B. | 钠与氧气反应的产物与反应条件有关 | |
| C. | 过氧化钠与水反应不能生成氢氧化钠 | |
| D. | 钠可以从四氯化钛中置换出钛 |
7.在恒温、体积为2L的密闭容器中加入1molCO2和3molH2,发生如下的反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0.可认定该可逆反应在一定条件下已达到化学平衡状态的是( )
| A. | 容器中CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1 | |
| B. | v正(CO2)=v逆(H2O) | |
| C. | 容器内混合气体密度保持不变 | |
| D. | 3molH-H键断裂同时断裂3molH-O键 |
