题目内容
下列物质的电离方程式,不正确的是( )
A、NaHCO3═H++CO
| ||
B、HNO3═H++NO
| ||
C、NaHSO4═H++SO
| ||
D、Al2(SO4)3=2Al3++3SO
|
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:A.碳酸氢钠在溶液中电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开;
B.硝酸为强酸,在溶液中完全电离出酸根离子和氢离子;
C.硫酸氢钠在溶液中完全电离出钠离子、氢离子和硫酸根离子,溶液中不存在硫酸氢根离子;
D.Al2(SO4)3为强电解质,在溶液中完全电离.
B.硝酸为强酸,在溶液中完全电离出酸根离子和氢离子;
C.硫酸氢钠在溶液中完全电离出钠离子、氢离子和硫酸根离子,溶液中不存在硫酸氢根离子;
D.Al2(SO4)3为强电解质,在溶液中完全电离.
解答:
解:A.碳酸氢钠在溶液中电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开,其电离方程式为:NaHCO3═HCO3-+Na+,故A错误;
B.硝酸为强酸,在溶液中完全电离出酸根离子和氢离子,其电离方程式为:HNO3═H++NO3-,故B正确;
C.硫酸氢钠在溶液中完全电离出钠离子、氢离子和硫酸根离子,溶液中不存在硫酸氢根离子,其电离方程式为:NaHSO4═H++SO42-+Na+,故C正确;
D.Al2(SO4)3为强电解质,在溶液中完全电离,其电离方程式为:Al2(SO4)3=2Al3++3SO42-,故D正确.
故选A.
B.硝酸为强酸,在溶液中完全电离出酸根离子和氢离子,其电离方程式为:HNO3═H++NO3-,故B正确;
C.硫酸氢钠在溶液中完全电离出钠离子、氢离子和硫酸根离子,溶液中不存在硫酸氢根离子,其电离方程式为:NaHSO4═H++SO42-+Na+,故C正确;
D.Al2(SO4)3为强电解质,在溶液中完全电离,其电离方程式为:Al2(SO4)3=2Al3++3SO42-,故D正确.
故选A.
点评:本题考查了电离方程式的书写判断,题目难度不大,注意掌握强电解质、弱电解质的判断方法,明确电离方程式的书写原则为解答关键,试题培养了学生规范答题的能力.

练习册系列答案
相关题目
下列说法正确的是( )
| A、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| B、若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数一定为m+11 |
| C、在BrCH=CHBr分子中,C-Br键采用的成键轨道是sp-p |
| D、由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,可能是含有共价键的离子化合物 |
下列现象或应用中,不能用胶体知识解释的是( )
| A、在饱和FeCl3溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
| B、用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 |
| C、清晨,在茂密的树林,常常可以看到从枝叶间透过的一道道光柱 |
| D、肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
下列有关表述不正确的是( )
A、-OH与 组成元素相同,含有的电子数也相同 组成元素相同,含有的电子数也相同 |
B、丙烷的分子结构模型示意图: |
C、次氯酸的电子式为 |
| D、熔化时NaHSO4的电离方程式为NaHSO4═Na++HSO4- |
下列四种模型仅由C、H、O三种原子组成,下列说法正确的是( )
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  | 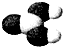 |
| A、模型1对应的物质含有双键 |
| B、1mol模型2对应的物质与足量的银氨溶液充分反应,能生成216gAg |
| C、模型3对应的物质在一定条件下能发生银镜反应 |
| D、模型3、模型4对应的物质均具有酸性,且酸性4强于3 |
用惰性电极实现电解,下列说法正确的是( )
| A、电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |
| B、电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 |
| C、电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为2:1 |
| D、电解氯化铜溶液,在阴极上和阳极上析出产物的质量之比为71:64 |