题目内容
下列说法正确的是( )
| A、除稀有气体外的非金属元素都能生成不同价态的含氧酸 |
| B、若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数一定为m+11 |
| C、在BrCH=CHBr分子中,C-Br键采用的成键轨道是sp-p |
| D、由IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,可能是含有共价键的离子化合物 |
考点:元素周期表的结构及其应用,元素周期律的作用,离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:A.O、F没有含氧酸;
B.ⅡA某元素的原子序数为m,若在短周期时同周期ⅢA元素的原子序数为m+1;
C.BrCH=CHBr分子中,C-Br为共价单键,Br的p轨道与C的杂化轨道成键;
D.IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,为Na2O2.
B.ⅡA某元素的原子序数为m,若在短周期时同周期ⅢA元素的原子序数为m+1;
C.BrCH=CHBr分子中,C-Br为共价单键,Br的p轨道与C的杂化轨道成键;
D.IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,为Na2O2.
解答:
解:A.O、F没有含氧酸,有正价的非金属元素能生成不同价态的含氧酸,故A错误;
B.ⅡA某元素的原子序数为m,若在短周期时同周期ⅢA元素的原子序数为m+1,在4、5周期相差11,在6、7周期相差25,故B错误;
C.BrCH=CHBr分子中,C-Br为共价单键,Br的p轨道与C的sp2轨道成键,故C错误;
D.IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,为Na2O2,含共价键和离子键,为离子化合物,故D正确,
故选D.
B.ⅡA某元素的原子序数为m,若在短周期时同周期ⅢA元素的原子序数为m+1,在4、5周期相差11,在6、7周期相差25,故B错误;
C.BrCH=CHBr分子中,C-Br为共价单键,Br的p轨道与C的sp2轨道成键,故C错误;
D.IA族和VIA族元素形成的原子个数比为1:1、电子总数为38的化合物,为Na2O2,含共价键和离子键,为离子化合物,故D正确,
故选D.
点评:本题考查较综合,涉及元素的性质、元素周期表结构及应用、化学键及杂化成键等,综合性较强,把握元素周期表及元素的性质为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列说法不正确的是( )
| A、用四氯化碳可以萃取乙酸水溶液中的乙酸 |
| B、元素分析可以鉴定有机物的实验式 |
| C、红外光谱分析可以鉴定有机物中含有的官能团或化学键 |
| D、核磁共振氢谱分析可以鉴定有机物中不同化学环境的氢原子及它们的数目比 |
下列说法正确的是( )
| A、氯水具有漂白作用,则氯水可使橙色的溴水褪为无色 |
| B、将氟气通入NaBr溶液中,可使溶液变橙色 |
| C、在某溶液中加入硝酸银溶液,出现黄色沉淀,说明该溶液中一定含有I- |
| D、溴水中加入一定量的Na2CO3粉末,溴水的颜色将变为无色 |
下列有关化学能与热能的说法正确的是( )
| A、中和反应属于吸热反应 |
| B、若某反应的反应物的总能量大于生成物的总能量,则该反应为吸热反应 |
| C、吸热反应是指需要加热才能进行的反应 |
| D、H2与Cl2的反应过程中,分子先转化为原子是吸收能量的过程,然后原子转化为新的分子是放出能量的过程 |
下列物质的电离方程式,不正确的是( )
A、NaHCO3═H++CO
| ||
B、HNO3═H++NO
| ||
C、NaHSO4═H++SO
| ||
D、Al2(SO4)3=2Al3++3SO
|
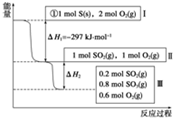 恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题:
恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题: