题目内容
下列四种模型仅由C、H、O三种原子组成,下列说法正确的是( )
| 序号 | 1 | 2 | 3 | 4 |
| 模型示意图 |  |  |  | 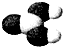 |
| A、模型1对应的物质含有双键 |
| B、1mol模型2对应的物质与足量的银氨溶液充分反应,能生成216gAg |
| C、模型3对应的物质在一定条件下能发生银镜反应 |
| D、模型3、模型4对应的物质均具有酸性,且酸性4强于3 |
考点:球棍模型与比例模型,甲醛,羧酸简介
专题:有机物的化学性质及推断
分析:由图知1为甲醇,2是甲醛,3是甲酸,4是碳酸,甲酸酸性大于碳酸,根据各自结构和性质分析.
解答:
解:A.甲醇不含双键,故A错误;
B.甲醛分子中相当于含有两个醛基,1mol甲醛可生成4mol银,能生成432gAg,故B错误;
C.甲酸分子的结构式为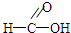 ,含有的原子团为:-COOH 羧基、-OH 羟基、OHC-醛基,故在一定条件下能发生银镜反应,故C正确;
,含有的原子团为:-COOH 羧基、-OH 羟基、OHC-醛基,故在一定条件下能发生银镜反应,故C正确;
D.3是甲酸,4是碳酸,甲酸酸性大于碳酸,故D错误.
故选C.
B.甲醛分子中相当于含有两个醛基,1mol甲醛可生成4mol银,能生成432gAg,故B错误;
C.甲酸分子的结构式为
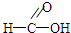 ,含有的原子团为:-COOH 羧基、-OH 羟基、OHC-醛基,故在一定条件下能发生银镜反应,故C正确;
,含有的原子团为:-COOH 羧基、-OH 羟基、OHC-醛基,故在一定条件下能发生银镜反应,故C正确;D.3是甲酸,4是碳酸,甲酸酸性大于碳酸,故D错误.
故选C.
点评:本题考查球棍模型,难度不大,易错选B按1个醛基计算.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
下列溶液中,溶质的物质的量浓度为1mol?L-1 的是( )
| A、将40 g NaOH溶于1 L 水所得的溶液 |
| B、将0.5 mol?L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液 |
| C、将31 g Na2O 溶于水并配成1 L的溶液 |
| D、含K+为1mol?L-1的K2SO4溶液 |
下列物质的电离方程式,不正确的是( )
A、NaHCO3═H++CO
| ||
B、HNO3═H++NO
| ||
C、NaHSO4═H++SO
| ||
D、Al2(SO4)3=2Al3++3SO
|
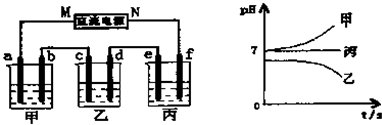
在三个不同密闭容器中分别充入NH3、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(P)从大到小的顺序是( )
| A、P(NH3)>P(H2)>P(O2) |
| B、P(O2)>P(NH3)>P(H2) |
| C、P(H2)>P(O2)>P(NH3) |
| D、P(H2)>P(NH3)>P(O2) |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、非标准状况下,1mol任何气体的体积不可能为22.4L |
| B、氨气的摩尔质量和NA个氨分子的质量在数值上相等 |
| C、标准状况下,NA个水分子所占的体积为22.4L |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
下列说法正确的是( )
| A、气体的摩尔体积约为22.4L?mol-1 |
| B、1 mol H2的质量是2g,它所占的体积约是22.4L?mol-1 |
| C、在标准状况下,1 mol任何物质所占的体积都约为22.4L?mol-1 |
| D、在标准状况下,1 mol任何气体所占的体积都约为22.4L |
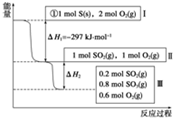 恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题:
恒温,容积为1L恒容条件下,硫可以发生如下转化,其反应过程和能量关系如图所示(已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1),请回答下列问题: