题目内容
选择H、O、S、Na四种元素中的适当的元素,组成符合下列要求的物质,将其化学式填入空格中.
(1)一种非金属单质
(2)一种非金属氧化物
(3)一种可溶性碱
(4)一种可溶性盐 .
(1)一种非金属单质
(2)一种非金属氧化物
(3)一种可溶性碱
(4)一种可溶性盐
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:(1)根据非金属单质是由非金属元素组成的来解答;
(2)根据氧化物是由两种元素组成,且其中一种为氧元素,非金属氧化物中另一种为元素为非金属;
(3)根据碱的概念可知,利用碱中有金属阳离子和OH-离子构成来解答;
(4)根据钠盐都溶于水,主要利用提供的元素来组成酸根离子.
(2)根据氧化物是由两种元素组成,且其中一种为氧元素,非金属氧化物中另一种为元素为非金属;
(3)根据碱的概念可知,利用碱中有金属阳离子和OH-离子构成来解答;
(4)根据钠盐都溶于水,主要利用提供的元素来组成酸根离子.
解答:
解:(1)氧元素为非金属元素,则由氧元素组成的非金属单质为氧气,故答案为:O2;
(2)非金属氧化物由非金属元素和氧元素组成,如水是由氢元素和氧元素组成的,故答案为:H2O;
(3)因碱中有金属阳离子和OH-离子,则根据提供的元素可知一定有钠离子和OH-离子,故答案为:NaOH;
(4)因钠盐都溶于水,S、H、O可组成SO4、HSO3等酸根,故答案为:Na2SO4(或NaHSO3).
(2)非金属氧化物由非金属元素和氧元素组成,如水是由氢元素和氧元素组成的,故答案为:H2O;
(3)因碱中有金属阳离子和OH-离子,则根据提供的元素可知一定有钠离子和OH-离子,故答案为:NaOH;
(4)因钠盐都溶于水,S、H、O可组成SO4、HSO3等酸根,故答案为:Na2SO4(或NaHSO3).
点评:本题考查学生对物质组成的认识,学生应能根据提供的元素结合习题中的要求书写符合物质类别的物质,并注意书写物质的化学式,题目难度不大.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
下列物质的电离方程式,不正确的是( )
A、NaHCO3═H++CO
| ||
B、HNO3═H++NO
| ||
C、NaHSO4═H++SO
| ||
D、Al2(SO4)3=2Al3++3SO
|
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、非标准状况下,1mol任何气体的体积不可能为22.4L |
| B、氨气的摩尔质量和NA个氨分子的质量在数值上相等 |
| C、标准状况下,NA个水分子所占的体积为22.4L |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
下列物质中,属于有机物但不属于烃的是( )
| A、CO2 |
| B、CH3COOH |
| C、Na2CO3 |
| D、CH4 |
下列说法正确的是( )
| A、气体的摩尔体积约为22.4L?mol-1 |
| B、1 mol H2的质量是2g,它所占的体积约是22.4L?mol-1 |
| C、在标准状况下,1 mol任何物质所占的体积都约为22.4L?mol-1 |
| D、在标准状况下,1 mol任何气体所占的体积都约为22.4L |
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,这项研究曾获2002年诺贝尔化学奖.下面有关13C、15N叙述正确的是( )
| A、13C与15N有相同的中子数 |
| B、13C与金钢石互为同素异形体 |
| C、15N 与14N 互为同位素 |
| D、15N的核外电子数与中子数相同 |
下列表格中烷烃的一氯代物只有一种,仔细分析其结构和组成的变化规律,判断第4位烷烃的分子式是( )
 | 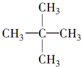 | 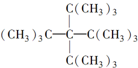 | … |
| 1 | 2 | 3 | … |
| A、C53H108 |
| B、C36H72 |
| C、C53H106 |
| D、C36H70 |
将甲烷和氧气的混合气体充入含有23.4g Na2O2的密闭容器中,保持容器中温度为150℃,用电火花引燃充分反应后,压强为0Pa,若将残留物溶于水,无气体逸出.据此判断下列叙述正确的是( )
| A、原混合气体中甲烷和氧气体积比为1:2 |
| B、原混合气体中甲烷和氧气体积比为2:1 |
| C、残留固体中只有NaOH |
| D、残留固体中只有Na2CO3 |