题目内容
11.在某无色、透明的强酸性溶液中,能大量共存的离子组是( )| A. | NH4+、NO3-、Al3+、Cl- | B. | K+、SO42-、Ba2+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | H+、SO42-、HCO3-、Na+ |
分析 强酸溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答 解:A.该组离子之间不反应,可大量共存,且离子均为无色,故A选;
B.SO42-、Ba2+结合生成沉淀,不能共存,故B不选;
C.MnO4-为紫色,与无色不符,故C不选;
D.H+、HCO3-结合生成水和气体,不能共存,故D不选;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
1.有关Na、Mg两种元素的性质叙述正确的是( )
| A. | 金属性:Na<Mg | |
| B. | 原子半径:Na>Mg | |
| C. | 单质的还原性:Na<Mg | |
| D. | 最高价氧化物对应水化物的碱性:NaOH<Mg(OH)2 |
19.下列用品的有效成分及用途对应错误的是( )
| A. | 用品: 有效成分:NaCl用途:做调味品 有效成分:NaCl用途:做调味品 | |
| B. | 用品: 有效成分:Na2CO3用途:做发酵粉 有效成分:Na2CO3用途:做发酵粉 | |
| C. | 用品: 有效成分:Al(OH)3用途:做抗酸药 有效成分:Al(OH)3用途:做抗酸药 | |
| D. | 用品: 有效成分:Ca(ClO)2用途:做消毒剂 有效成分:Ca(ClO)2用途:做消毒剂 |
6.下列过程中化学键未被破坏的是( )
| A. | NaCl固体溶于水 | B. | NH4Cl受热分解 | C. | 干冰升华 | D. | SO2气体溶于水 |
16.己知丙烷的燃烧热△H=-2200KJ•mol-1,若一定量的丙烷(C3H8)完全燃烧后生成18g水,则放出的热量约为( )
| A. | 55 kJ | B. | 220 kJ | C. | 1108 kJ | D. | 550 kJ |
3.关于阿伏伽德罗常数NA,下列说法正确的是( )
| A. | 0.5mol.L-1硫酸钠溶液中含有溶质离子总数为1.5NA | |
| B. | 标准状况下,22.4L甲醇完全燃烧产生NA个CO2分子 | |
| C. | 常温常压下,46g NO2、N2O4混合物中,分子数为NA | |
| D. | 常温常压下,N2和O2混合气体22.4L所含的分子数少于6.02×1023 |
20.已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2.下列有关离子反应或离子方程式的叙述中,正确的是( )
| A. | 向0.1molFeI2溶液中滴加少量氯水,反应中有0.3mol电子转移 | |
| B. | 向溴水中加入足量氯化亚铁能使溶液变成无色 | |
| C. | 向NaClO溶液中通入少量CO2的离子方程式:ClO-+CO2+H2O═HClO+HCO3- | |
| D. | 能使pH试纸显深红色的溶液,Fe3+、Cl-、Ba2+、Br-能大量共存 |
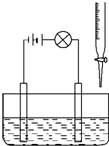 在烧杯里加入20mL 0.1mol/L的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):
在烧杯里加入20mL 0.1mol/L的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如图(夹持仪器已去掉):