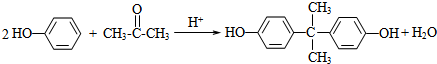题目内容
14.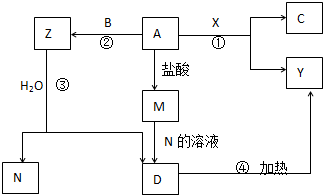 如图转化关系中,A、B、C为单质,其余方框内均为化合物,B、X、N常温下为气体,C为黑色固体,D为白色沉淀,A、Y、Z、M、D中均含同一种元素(框图中某些生成物已略去).请填写下列空白:
如图转化关系中,A、B、C为单质,其余方框内均为化合物,B、X、N常温下为气体,C为黑色固体,D为白色沉淀,A、Y、Z、M、D中均含同一种元素(框图中某些生成物已略去).请填写下列空白:(1)完成下列化学方程式:
①2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C
②3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
③Mg3N2+6H2O=3Mg(OH)2+2NH3↑
④Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O
(2)试拟定工业上由Y制取单质A的反应原理(用化学方程式表示)MgO+2HCl=MgCl2+H2O,MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
分析 A、Y、Z、M、D中均含同一种元素,C为黑色固体单质,则C为C,A单质与气体X反应生成C,且A能与盐酸反应,则A为Mg,所以X为CO2,Y为MgO,A与盐酸反应生成M为Mg(OH)2,M与N反应生成D,D加热分解生成Y,所以N为碱性溶液,D为白色沉淀,D为Mg(OH)2,根据A与气体B反应生成Z,Z与水反应生成气体N和氢氧化镁,可推知Z为Mg3N2,B为N2,N为NH3,据此答题.
解答 解:A、Y、Z、M、D中均含同一种元素,C为黑色固体单质,则C为C,A单质与气体X反应生成C,且A能与盐酸反应,则A为Mg,所以X为CO2,Y为MgO,A与盐酸反应生成M为Mg(OH)2,M与N反应生成D,D加热分解生成Y,所以N为碱性溶液,D为白色沉淀,D为Mg(OH)2,根据A与气体B反应生成Z,Z与水反应生成气体N和氢氧化镁,可推知Z为Mg3N2,B为N2,N为NH3,
(1)根据上面的分析可知,反应①的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,反应②的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2,反应③的化学方程式为Mg3N2+6H2O=3Mg(OH)2+2NH3↑,反应④的化学方程式为Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;Mg3N2+6H2O=3Mg(OH)2+2NH3↑;Mg(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+H2O;
(2)工业上由MgO制取单质Mg,可以用氧化镁与盐酸反应生成氯化镁,再电解氯化镁生成镁,反应的化学方程式表示为MgO+2HCl=MgCl2+H2O,MgCl2 $\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑,
故答案为:MgO+2HCl=MgCl2+H2O;MgCl2 $\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑.
点评 本题考查了物质转化关系分析判断,此类题目考查学生对元素化合物知识的熟悉程度,同时很好的考查学生的逻辑推理能力合整体思维能力,题目难度中等.

| A. | 食盐可作调味剂,也可用作食品防腐剂 | |
| B. | 二氧化硫可用于制作葡萄酒的食品添加剂 | |
| C. | 还原铁粉和生石灰均可用作食品包装袋内的脱氧剂 | |
| D. | “地沟油”禁止食用,但可用来制取肥皂 |
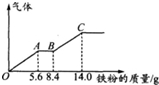 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )| A. | NO,1.5mol/L | B. | H2,1.5mol/L | C. | NO,2.5mol/L | D. | H2,2.5mol/L |
①NH3和H2O
②NH4+和H3O+
③NH3和H3O+
④O3和SO2
⑤CO2和BeCl2
⑥NH4+和SO42-
⑦BF3和Al2Cl6.
| A. | 全部 | B. | 除④⑥⑦以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
| A. | 100mL1mol/L的碳酸钠溶液中含有CO32-为1NA | |
| B. | 常温、常压下,0.5mol臭氧中含有氧原子为1.5NA | |
| C. | 标准状况下,1mol NO2气体与水反应生成NO3-为NA | |
| D. | 78gNa2O2中含有O2-为2NA |
| A. | 家用燃气灶是化学能转化为热能的应用装置 | |
| B. | 食品放入冰箱中,因为温度低,变质速率降低,所以食品能够保存较长时间 | |
| C. | 将煤气化,有利于提供更多的能量,而且有效地减少温室气体的产生 | |
| D. | 因为食用醋中含有酸,可以用来清洗锅垢 |
| A. | 标准状况下,1.12 L的H2O所含的原子数必大于1.5×6.02×1023 | |
| B. | 含有相同氧原子数的SO2和CO2的物质的量相等 | |
| C. | 常温常压下,48 g O3中含有的氧原子数为3NA | |
| D. | 标准状况下,2.24 L NH3和CH4的混合气体,所含电子总数为2NA |
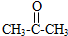 )在酸性介质中反应制得.写出反应的化学方程式
)在酸性介质中反应制得.写出反应的化学方程式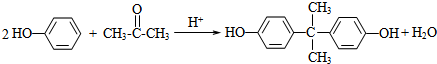
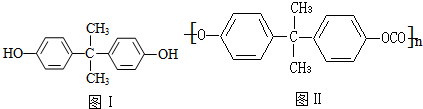
 )为原料合成一种防碎塑料--聚碳酸酯,简称PC结构简式如图Ⅱ.以PC为原料制成的婴儿奶瓶在使用过程中会析放出极少量的双酚A,长期使用可能损害婴儿的健康.
)为原料合成一种防碎塑料--聚碳酸酯,简称PC结构简式如图Ⅱ.以PC为原料制成的婴儿奶瓶在使用过程中会析放出极少量的双酚A,长期使用可能损害婴儿的健康.