题目内容
5.下列叙述中,错误的是( )| A. | 新制氯水的氧化性强于久置氯水 | |
| B. | 过量铁与Cl2反应时生成FeCl2 | |
| C. | 1molCl2与热NaOH溶液反应生成NaClO3和NaCl时,需NaOH 2mol | |
| D. | 将饱和氯水滴到淀粉碘化钾试纸上,试纸先变蓝后变白,说明氯水具有强氧化性 |
分析 A.新制氯水中含有大量HClO,久置的氯水中,HClO分解生成HCl和O2,久置的氯水中次氯酸含量降低;
B.过量铁与Cl2反应生成FeCl3;
C.根据氯原子和钠原子守恒计算;
D.氯气与水反应生成次氯酸,次氯酸具有强氧化性而使蓝色试纸变白.
解答 解:A.新制氯水中含有大量HClO,久置的氯水中,HClO分解生成HCl和O2,久置的氯水中次氯酸含量降低,次氯酸具有强氧化性,所以新制氯水的氧化性强于久置氯水,故A正确;
B.因为氯气具有强氧化性,则过量铁与Cl2反应只生成FeCl3,故B错误;
C.1molCl2与热NaOH溶液反应生成NaClO3和NaCl,因为生成物中氯原子与钠原子按1:1组成,根据氯原子和钠原子守恒,所以消耗NaOH为2mol,故C正确;
D.将新制饱和氯水滴到淀粉碘化钾试纸上,试纸先变蓝后变白,是因为氯气和碘化钾反应生成碘单质,遇到淀粉变蓝色,氯气与水反应生成次氯酸,次氯酸具有强氧化性而使蓝色试纸变白,故D正确;
故选B.
点评 本题考查氯气及其氯水的成分和性质,题目难度不大,注意氯气与水反应生成次氯酸,次氯酸具有强氧化性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.FeS溶于盐酸,CuS不溶于盐酸而溶于硝酸,主要是因为( )
| A. | 水解能力不同 | B. | Ksp不同 | C. | 溶解的速度不同 | D. | 酸碱性不同 |
16.化学与生活、生产密切相关,下列有关说法正确的是( )
| A. | 某同学的体检报告单显示其血液中葡萄糖含量为4.94mmol/L,mmol/L是物质的量的单位 | |
| B. | 石油是复杂的混合物,通过分馏可以获得汽油、煤油等,通过催化重整可以获得乙烯、丙烯等 | |
| C. | 自然界中的方铅矿(PbS),遇上CuSO4溶液会慢慢变成铜蓝(CuS)说明Ksp(PbS)>Ksp(CuS) | |
| D. | 水玻璃是制备木材防火剂的原料,其主要成分是二氧化硅 |
13.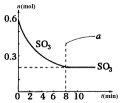 在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )
在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )
 在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )
在一个2L的密闭容器中,发生反应:2SO3(g)?2SO2(g)+O2(g)-Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是( )| A. | 0~8min内v(SO3)=0.025mol/(L•min) | |
| B. | 8min时,v逆(SO2)=2v正 (O2) | |
| C. | 8min时,容器内压强保持不变 | |
| D. | 若8min时将容器压缩为1L,n(SO3)的变化如图中a |
20.锌与稀硫酸反应,下列说法错误的是( )
| A. | 加热可加快反应速率 | B. | 增大稀硫酸的浓度可加快反应速率 | ||
| C. | 粉碎锌粒可加快反应速率 | D. | 提高锌的纯度可加快反应速率 |
10.《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”,“以烧酒复烧二次…价值数倍也”.其方法与分离下列物质的实验方法原理上相同的是( )
| A. | 甲苯和水 | B. | 硝酸钾和氯化钠 | C. | 乙酸乙酯和乙酸 | D. | 食盐水和泥沙 |
17.下列实验操作正确的是( )
| A. | 可用长颈漏斗分离汽油和水的混合液 | |
| B. | 酒精灯使用不当引起少量酒精在桌上燃烧时,立即用湿布盖灭 | |
| C. | 给盛有液体的试管加热时,要不停地移动试管 | |
| D. | 洗净的锥形瓶和容量瓶可用烘箱烘干 |
14.某有机物的结构简式为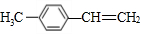 ,其分子结构中处在同一平面内的原子最多有( )
,其分子结构中处在同一平面内的原子最多有( )
 ,其分子结构中处在同一平面内的原子最多有( )
,其分子结构中处在同一平面内的原子最多有( )| A. | 15个 | B. | 16个 | C. | 17个 | D. | 18个 |
14.下列有关实验室一般事故的预防和处理方法正确的是( )
| A. | 燃着的酒精灯打翻失火,立即用水浇灭 | |
| B. | 若不慎将浓碱液沾在皮肤上,立即用大量水冲洗,再涂上适量的稀硼酸溶液 | |
| C. | 用氢气还原氧化铜时,先加热再通入氢气,以免浪费氢气 | |
| D. | 配制稀硫酸时,可先在量筒中加入一定量的水,再在搅拌下缓慢加入浓硫酸 |