题目内容
20.锌与稀硫酸反应,下列说法错误的是( )| A. | 加热可加快反应速率 | B. | 增大稀硫酸的浓度可加快反应速率 | ||
| C. | 粉碎锌粒可加快反应速率 | D. | 提高锌的纯度可加快反应速率 |
分析 增大反应物接触面积、适当增大稀硫酸浓度、升高温度等都能增大反应速率,据此分析解答.
解答 解:A、温度越高反应速率越快,故A正确;
B、浓度越大反应速率越快,所以增大稀硫酸的浓度可加快反应速率,故B正确;
C、增加反应的接触面积加快反应速率,所以粉碎锌粒可加快反应速率,故C正确;
D、粗锌可形成原电池反应而加快反应速率,而改用纯度高的锌粒,反应速率减小,故D错误;
故选D.
点评 本题考查反应速率的因素,为高频考点,把握影响反应速率的常见因素为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
11.化学与生产、生活、社会密切相关,下列有关说法中正确的是( )
| A. | 用K2FeO4代替Cl2处理饮用水,既有杀菌消毒作用,又有净水作用 | |
| B. | 古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中提取青蒿素是利用氧化还原反应原理 | |
| C. | 面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物合物,也属于离子化合物,其阴阳离子冷数比为2:l,过氧化苯甲酞属于有机物 | |
| D. | 二氧化硫有毒,产禁将其添加到任何食品和饮料中 |
15.对稳定人体血液的pH起重要作用的离子是( )
| A. | Na+ | B. | HCO3- | C. | Fe2+ | D. | Cl- |
5.下列叙述中,错误的是( )
| A. | 新制氯水的氧化性强于久置氯水 | |
| B. | 过量铁与Cl2反应时生成FeCl2 | |
| C. | 1molCl2与热NaOH溶液反应生成NaClO3和NaCl时,需NaOH 2mol | |
| D. | 将饱和氯水滴到淀粉碘化钾试纸上,试纸先变蓝后变白,说明氯水具有强氧化性 |
12.X、Y、Z、M、W为五种短周期主族元素,X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物溶于水后溶液呈碱性;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 简单的离子半径:W>Z>Y>X | |
| B. | 五种元素中只有X存在同素异形体 | |
| C. | W和M形成的化合物是离子化合物 | |
| D. | 工业上采用电解W和Z形成的化合物制备W单质 |
9.短周期元素R、T、X、Y、Z在元素周期表的相对位置如表所示,它们的最外层电子数之和为24.则下列判断正确的是( )
| R | T | |
| X | Y | Z |
| A. | R位于元素周期表中第二周期第VA族 | |
| B. | R能分别与X、Z形成共价化合物 | |
| C. | 原子半径大小顺序为X>T>Y | |
| D. | Z元素的最高价氧化物对应的水化的化学式为HZO4 |
 已知A、B、C、D、X、Y、Z七种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数比Y的最外层电子数多1.C原子的最外层电子数是次外层电子数的3倍,D原子半径在同周期中除稀有气体外最大,X是同周期中简单离子半径最小的元素.请回答下列问题:
已知A、B、C、D、X、Y、Z七种短周期主族元素的原子序数依次增大,A是元素周期表中原子半径最小的,B的最高价氧化物的水化物与其氢化物反应生成盐,且B的核电荷数比Y的最外层电子数多1.C原子的最外层电子数是次外层电子数的3倍,D原子半径在同周期中除稀有气体外最大,X是同周期中简单离子半径最小的元素.请回答下列问题: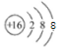 ,A与C形成的10电子分子的电子式为
,A与C形成的10电子分子的电子式为 .
.