题目内容
下列离子方程式中,正确的有( )个
(1)澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O
(2)氢氧化钡与硫酸反应:OH-+H+═H2O
(3)铜片与硝酸银溶液反应:Cu+Ag+═Cu2++Ag
(4)氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-═Mg(OH)2↓
(5)铁片投入稀盐酸中:2Fe+6H+═2Fe3++3H2↑
(6)氨水与盐酸的反应:OH-+H+═H2O
(7)碳酸氢钠与盐酸反应:HCO3-+H+═CO2↑+H2O
(8)Na2O与水反应:O2-+H2O═2OH-
(9)少量的NH4HSO4溶液与Ba(OH)2溶液的反应:NH4++H++SO42-+Ba2++2OH-═NH3.H2O+H2O+BaSO4↓
(10)向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓
(1)澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H2O
(2)氢氧化钡与硫酸反应:OH-+H+═H2O
(3)铜片与硝酸银溶液反应:Cu+Ag+═Cu2++Ag
(4)氯化镁溶液与氢氧化钠溶液反应:Mg2++2OH-═Mg(OH)2↓
(5)铁片投入稀盐酸中:2Fe+6H+═2Fe3++3H2↑
(6)氨水与盐酸的反应:OH-+H+═H2O
(7)碳酸氢钠与盐酸反应:HCO3-+H+═CO2↑+H2O
(8)Na2O与水反应:O2-+H2O═2OH-
(9)少量的NH4HSO4溶液与Ba(OH)2溶液的反应:NH4++H++SO42-+Ba2++2OH-═NH3.H2O+H2O+BaSO4↓
(10)向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓
| A、1 | B、2 | C、3 | D、4 |
考点:离子方程式的书写
专题:
分析:(1)澄清石灰水与稀盐酸反应,生成氯化钙和水,氢氧化钙在离子反应中完全电离;
(2)漏写生成硫酸钡的离子反应;
(3)电子、电荷不守恒;
(4)氯化镁溶液与氢氧化钠溶液反应,生成氢氧化镁和氯化钠;
(5)铁片投入稀盐酸中,反应生成氯化亚铁和氢气;
(6)氨水与盐酸的反应,生成氯化铵,一水合氨在离子反应中保留化学式;
(7)碳酸氢钠与盐酸反应,生成氯化钠、水、二氧化碳;
(8)Na2O在离子反应中保留化学式;
(9)少量的NH4HSO4溶液与Ba(OH)2溶液的反应,生成硫酸钡、水、一水合氨;
(10)向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性,生成硫酸钡、硫酸钠和水.
(2)漏写生成硫酸钡的离子反应;
(3)电子、电荷不守恒;
(4)氯化镁溶液与氢氧化钠溶液反应,生成氢氧化镁和氯化钠;
(5)铁片投入稀盐酸中,反应生成氯化亚铁和氢气;
(6)氨水与盐酸的反应,生成氯化铵,一水合氨在离子反应中保留化学式;
(7)碳酸氢钠与盐酸反应,生成氯化钠、水、二氧化碳;
(8)Na2O在离子反应中保留化学式;
(9)少量的NH4HSO4溶液与Ba(OH)2溶液的反应,生成硫酸钡、水、一水合氨;
(10)向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性,生成硫酸钡、硫酸钠和水.
解答:
解:(1)澄清石灰水与稀盐酸反应的离子反应为OH-+H+═H2O,故错误;
(2)氢氧化钡与硫酸反应的离子反应为2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故错误;
(3)铜片与硝酸银溶液反应的离子反应为Cu+2Ag+═Cu2++2Ag,故错误;
(4)氯化镁溶液与氢氧化钠溶液反应的离子反应为Mg2++2OH-═Mg(OH)2↓,故正确;
(5)铁片投入稀盐酸中的离子反应为Fe+2H+═Fe2++H2↑,故错误;
(6)氨水与盐酸的反应的离子反应为NH3.H2O+H+═H2O+NH4+,故错误;
(7)碳酸氢钠与盐酸反应的离子反应为HCO3-+H+═CO2↑+H2O,故正确;
(8)Na2O与水反应的离子反应为Na2O+H2O═2OH-+2Na+,故错误;
(9)少量的NH4HSO4溶液与Ba(OH)2溶液的反应的离子反应为NH4++H++SO42-+Ba2++2OH-═NH3.H2O+H2O+BaSO4↓,故正确;
(10)向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性的离子反应为2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故正确;
故选D.
(2)氢氧化钡与硫酸反应的离子反应为2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故错误;
(3)铜片与硝酸银溶液反应的离子反应为Cu+2Ag+═Cu2++2Ag,故错误;
(4)氯化镁溶液与氢氧化钠溶液反应的离子反应为Mg2++2OH-═Mg(OH)2↓,故正确;
(5)铁片投入稀盐酸中的离子反应为Fe+2H+═Fe2++H2↑,故错误;
(6)氨水与盐酸的反应的离子反应为NH3.H2O+H+═H2O+NH4+,故错误;
(7)碳酸氢钠与盐酸反应的离子反应为HCO3-+H+═CO2↑+H2O,故正确;
(8)Na2O与水反应的离子反应为Na2O+H2O═2OH-+2Na+,故错误;
(9)少量的NH4HSO4溶液与Ba(OH)2溶液的反应的离子反应为NH4++H++SO42-+Ba2++2OH-═NH3.H2O+H2O+BaSO4↓,故正确;
(10)向NaHSO4溶液滴加Ba(OH)2溶液至溶液呈中性的离子反应为2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
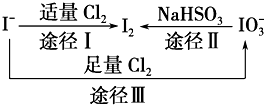 碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系(已知:NaHSO3做还原剂,被氧化为Na2SO4),根据图示转化关系推测下列说法不正确的是( )
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系(已知:NaHSO3做还原剂,被氧化为Na2SO4),根据图示转化关系推测下列说法不正确的是( )| A、海带中提取碘过程中,将I-氧化成I2所通入的Cl2不宜过量 |
| B、足量Cl2能使湿润的KI淀粉试纸先变蓝后变白的原因可能是:5Cl2+I2+6H2O═2HIO3+10HCl |
| C、由图可知氧化性的强弱顺序为Cl2>I2>IO3- |
| D、途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA |
下列反应的离子方程式中正确的是( )
| A、钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| B、氢氧化钡溶液和硫酸铵溶液反应:Ba2++SO42-=BaSO4↓ |
| C、硫化钠溶于水呈碱性:S2-+2H2O?H2S+2OH- |
| D、向溴化亚铁溶液中通入少量氯气:Cl2+2Br-=2Cl-+Br2 |
偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列有关偏二甲肼(C2H8N2)叙述正确的是( )
| A、偏二甲肼的摩尔质量为60g |
| B、1 mol偏二甲肼的质量为60g/mol |
| C、6.02×1023个偏二甲肼分子的质量为60g |
| D、6 g偏二甲肼含有NA个偏二甲肼分子 |
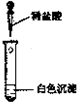
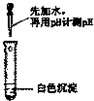
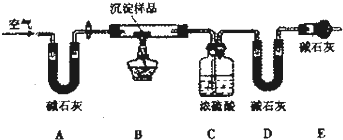
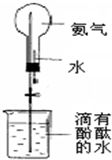 (1)写出实验室制取氨气的化学方程式:
(1)写出实验室制取氨气的化学方程式: