题目内容
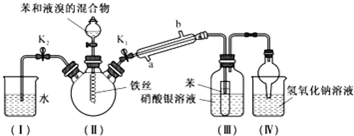
18.检验某溶液中是否含有 K+、Fe3+、Cl-、Mg2+、I-、CO32-、SO42-,限用的试剂有:盐酸、硫酸、硝酸银溶液、硝酸钡溶液.设计如下实验步骤,并记录相关现象.下列叙述不正确的是( )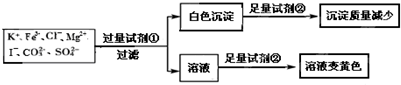
| A. | 试剂①为硝酸钡 | |
| B. | 试剂②一定为盐酸 | |
| C. | 该溶液中一定有 I-、CO32-、SO42-、K+ | |
| D. | 通过在黄色溶液中加入硝酸银溶液可以检验原溶液中是否存在Cl- |
分析 由实验可知,加试剂①为硝酸钡溶液,生成白色沉淀为碳酸钡和硫酸钡,则加试剂②为盐酸,沉淀减少,硫酸钡不溶于酸;加试剂①过滤后的滤液中,再加试剂②为盐酸,氢离子,硝酸根离子、I-发生氧化还原反应生成碘,溶液为黄色,以此来解答.
解答 解:由实验可知,加试剂①为硝酸钡溶液,生成白色沉淀为碳酸钡和硫酸钡,则加试剂②为盐酸,沉淀减少,硫酸钡不溶于酸,则原溶液中一定存在CO32-、SO42-,则不含Fe3+、Mg2+;加试剂①过滤后的滤液中,再加试剂②为盐酸,氢离子,硝酸根离子、I-发生氧化还原反应生成碘,溶液为黄色,溶液为电中性,则一定含阳离子为K+,
A.由上述分析可知,试剂①为硝酸钡,故A正确;
B.由上述分析可知,试剂②一定为盐酸,因碳酸钡与硫酸反应生成硫酸钡使沉淀量增加,故B正确;
C.由上述分析可知,该溶液中一定有I-、CO32-、SO42-、K+,故C正确;
D.黄色溶液中加入硝酸银可生成AgI沉淀,试剂②加盐酸引入氯离子,不能检验原溶液中是否存在Cl-,故D错误;
故选D.
点评 本题考查物质鉴别、检验的实验方案设计,为高频考点,把握白色沉淀的成分、黄色溶液中含碘为解答的关键,侧重分析与实验能力的考查,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.次氯酸的电子式为 ,则1mol该物质所含有的电子的物质的量是( )
,则1mol该物质所含有的电子的物质的量是( )
 ,则1mol该物质所含有的电子的物质的量是( )
,则1mol该物质所含有的电子的物质的量是( )| A. | 14mol | B. | 15mol | C. | 26mol | D. | 27mol |
13.某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如右图所示.则下列说法正确的是( )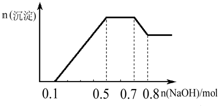

| A. | 溶液中的阳离子只有H+、Mg2+、Al3+ | |
| B. | 溶液中一定不含CO32-,一定含有SO42-和NO3- | |
| C. | 溶液中n(NH4+)=0.2 mol | |
| D. | 三种离子的物质的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1 |
3.下列各组物质中,常温下发生反应并放出红棕色气体的是( )
| A. | 铜和浓硫酸 | B. | 铜和浓硝酸 | C. | 铜和浓盐酸 | D. | 铁和稀硫酸 |
10.下列物质中存在顺反异构体的是( )
| A. | 2-氯丙烯 | B. | 1,2-二氯乙烯 | C. | 2-甲基-2-丁烯 | D. | 1-丁烯 |
7.下列检验Na2SO4溶液中是否含有Cl-的方法,正确的是( )
| A. | 先加BaCl2溶液,过滤后在滤液中再加AgNO3溶液 | |
| B. | 先加足量的Ba(NO3)2溶液,过滤后在滤液中再加AgNO3溶液和硝酸溶液 | |
| C. | 先加AgNO3溶液,过滤后,在沉淀中再加稀硝酸 | |
| D. | 先加足量的Ba(OH)2溶液,过滤后在滤液中再加AgNO3溶液 |
8.下列离子方程式不正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O | |
| B. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O$\stackrel{△}{→}$2C6H5OH+CO | |
| D. | 甲醛溶液与足量的银氨溶液共热HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O |