题目内容
6.下列盐,既可以用“碱性氧化物+酸”制取,也可以用“酸性氧化物+碱”制取的是( )| A. | KCl | B. | Na2S | C. | (NH4)2SO4 | D. | BaSO4 |
分析 A.氧化钾与盐酸可发生反应KCl;
B.氧化钠与氢硫酸反应生成硫化钠;
C.一水合氨与三氧化硫反应生成硫酸铵;
D.氧化钡与硫酸反应、氢氧化钡与三氧化硫均反应生成硫酸钡.
解答 解:A.KCl不能由“酸性氧化物+碱”制取,故A不选;
B.Na2S不能由“酸性氧化物+碱”制取,故B不选;
C.(NH4)2SO4不能由“碱性氧化物+酸”制取,故C不选;
D.BaSO4既可以用“碱性氧化物+酸”制取,也可以用“酸性氧化物+碱”制取,氧化钡与硫酸反应、氢氧化钡与三氧化硫均反应生成硫酸钡,故D选;
故选D.
点评 本题考查物质的性质及反应,为高频考点,把握酸、碱及氧化物的性质为解答的关键,侧重分析与应用能力的考查,注意发生的复分解反应,题目难度不大.

练习册系列答案
相关题目
17.在一定温度下,向aL密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(s)+2Y(g)?2Z(g),能判断该反应达平衡状态的是( )
| A. | 容器内气体压强不随时间变化 | |
| B. | 容器内气体密度不随时间变化 | |
| C. | 容器内X、Y、Z的浓度之比为1:2:2 | |
| D. | X的消耗速率和Z的生成速率之比为1:2 |
14.设NA为阿伏加德罗常数,下列说法不正确的是( )
| A. | 2.0g重水(D2O)中含有的中子数为NA | |
| B. | 标准状况下22.4L的四氯化碳,含有四氯化碳分子数为NA | |
| C. | 23g金属钠变为钠离子时失去的电子数为NA | |
| D. | 常温常压下,48gO3和O2混合气体中含有的氧原子数为3NA |
1.配置250mL0.5mol/L的NaCl溶液,有下列仪器:①托盘天平、②量筒、③烧杯、④玻璃棒、⑤漏斗、⑥500mL容量瓶、⑦药匙、⑧250mL容量瓶、⑨胶头滴管、⑩坩埚,需要用到的仪器有( )
| A. | ①③④⑦⑧⑨ | B. | ①④⑦⑧⑨⑩ | C. | ①③④⑥⑨⑩ | D. | ①②④⑤⑧⑨ |
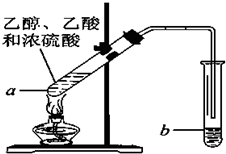 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题.
乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平.请回答下列问题. ,结构简式H2C=CH2.
,结构简式H2C=CH2. ,反应类型是加聚反应.
,反应类型是加聚反应.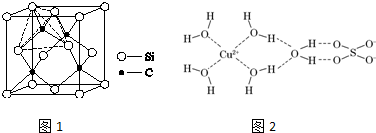
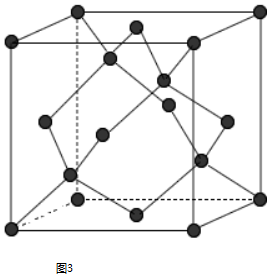
 ;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.
;亚铜离子(Cu+)基态时的电子排布式为1s22s22p63s23p63d10或[Ar]3d10.