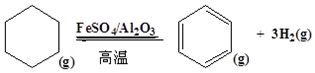题目内容
4.选择下列实验方法分离物质,将分离方法的序号填在横线上.A.萃取分液法 B.加热分解法 C.结晶法 D.分液法 E.蒸馏法 F.过滤法
(1)F分离饱和食盐水与沙子的混合物.
(2)C从KNO3和NaCl的混合溶液中获得KNO3.
(3)D分离水和汽油的混合物.
(4)E分离四氯化碳(沸点76.75℃)和甲苯(沸点110.6℃) 的混合物.(已知:四氯化碳和甲苯互溶)
(5)A从碘的水溶液里提取碘.
分析 (1)沙子不溶于水,食盐溶于水;
(2)二者溶解度受温度影响不同;
(3)水和汽油分层;
(4)二者互溶,但沸点不同;
(5)碘不易溶于水,易溶于有机溶剂.
解答 解:(1)沙子不溶于水,食盐溶于水,选择过滤法分离,故答案为:F;
(2)二者溶解度受温度影响不同,选择结晶法分离,故答案为:C;
(3)水和汽油分层,选择分液法分离,故答案为:D;
(4)二者互溶,但沸点不同,选择蒸馏法分离,故答案为:E;
(5)碘不易溶于水,易溶于有机溶剂,选择萃取分液法分离,故答案为:A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意分离方法的选择,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时,已知数据如表所示:
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的溶液的说法,比较合理的( )
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
| A. | 向该混合溶液中加入少量铁粉即能观察到红色固体析出 | |
| B. | 向该混合溶液中逐滴加入NaOH溶液,最先看到蓝色沉淀 | |
| C. | 该混合溶液中c(SO42-):{c(Cu2+)+c(Fe2+)+c(Fe3+)}>5:4 | |
| D. | 向该混合溶液中加入适量氯水,并调节pH为3~4,然后过滤,可得到纯净的CuSO4溶液 |
19.下列实验装置正确且能完成实验目的是( )
| A. |  测定一定时间内生成H2的反应速率 | B. |  提取海带中的碘 | ||
| C. |  检验火柴燃烧产生的SO2 | D. |  证明非金属性:Cl>C>Si |
16.下列说法或表示方法正确的是( )
| A. | 等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量一样多 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 在101kpa时,2gH2完全燃烧,生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ/mol | |
| D. | 在强酸强碱稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含1molNaOH的溶液和含0.5molH2SO4的浓硫酸混合,放出的热量大于57.3 kJ |
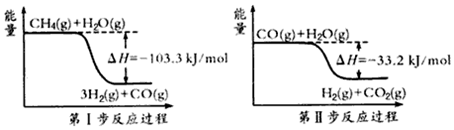
 硫-碘循环分解水制氢主要涉及下列反应:
硫-碘循环分解水制氢主要涉及下列反应: