题目内容
下列各项表达中正确的( )
A、N2的电子式: | ||
| B、106g的乙醇和丙醇混合液完全燃烧生成的CO2为112L(标准状况) | ||
C、邻羟基苯甲酸的结构简式: | ||
D、质子数为53,中子数为78的碘原子:
|
考点:电子式,核素,结构简式
专题:化学用语专题
分析:A.N2是以共价键作用结合成的单质分子,N原子间通过三对共用电子对结合;
B.根据极限法分别求出CO2的体积;
C. 为间羟基苯甲酸;
为间羟基苯甲酸;
D.质量数=质子数+中子数.
B.根据极限法分别求出CO2的体积;
C.
 为间羟基苯甲酸;
为间羟基苯甲酸;D.质量数=质子数+中子数.
解答:
解:A.N2是以共价键作用结合成的单质分子,N原子间通过三对共用电子对结合,N2的电子式为 ,故A错误;
,故A错误;
B.若全为乙醇,生成二氧化碳为
×2×22.4=103.2L;若全丙醇,生成二氧化碳为
×3×22.4=118.7L,所以106g的乙醇和丙醇混合液完全燃烧生成的CO2为的体积应介于两者之间,故B错误;
C.邻羟基苯甲酸,俗名水杨酸,其结构简式为 ,故C错误;
,故C错误;
D.质量数=质子数+中子数=53+78=131,故D正确.
故选D.
 ,故A错误;
,故A错误; B.若全为乙醇,生成二氧化碳为
| 106 |
| 46 |
| 106 |
| 60 |
C.邻羟基苯甲酸,俗名水杨酸,其结构简式为
 ,故C错误;
,故C错误;D.质量数=质子数+中子数=53+78=131,故D正确.
故选D.
点评:本题考查化学用语,难度不大,解题的关键是掌握并灵活运用原子中核电荷数=核内质子数=核外电子数、质量数=质子数+中子数.

练习册系列答案
相关题目
“神舟四号”的成功发射与回收,表明我国的载人航天技术已经有了突破性进展.在飞船的火箭推进器中常装有液态肼(用X表示)和液态双氧水(H2O2),它们混合时的反应方程式为:2H2O2+X=N2+4H2O,则肼(X)的化学式为( )
| A、N2H6 |
| B、N2H4 |
| C、NH2 |
| D、N2H4O2 |
二氧化氯(ClO2)是一种广谱、高效的消毒剂,易溶于水,尤其在水处理等方面有广泛应用.以下是某校化学研究小组设计实验室制取ClO2的工艺流程图.下列有关说法正确的是( )

A、电解时发生反应的化学方程式为:2HCl
| ||||
| B、由NaClO2溶液制取0.6mol ClO2时,至少消耗0.1mol NCl3 | ||||
| C、将产生的混合气体通过盛有碱石灰的干燥器以除去ClO2中的 NH3 | ||||
| D、溶液X的成分为NaClO3和NaOH |
下列各组中的性质比较中,不正确的是( )
| A、酸性 HClO4>HBrO4>HIO4 |
| B、碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C、还原性 F->Cl->Br- |
| D、稳定性 HCl>H2S>PH3 |
将14g铜银合金与足量某浓度的硝酸反应,使放出的气体与1.12L(标准状况)氧气混合恰好被水全部吸收生成硝酸,则合金中铜的质量为( )
| A、3.2g | B、4.43g |
| C、10.8g | D、12.4g |
在一定温度下,将X和Y 各0.16mol充入10L 恒容密闭容器中,发生反应:2X(g)+Y(s)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表下列说法正确的是( )
| t/s | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.10 | 0.09 | 0.09 |
| A、反应前2s的平均速率v(Z)=2.0×10-3 mol/(L?s) |
| B、其他条件不变,加入一定量的Y,反应速率一定加快 |
| C、反应进行4s时,X的转化率75% |
| D、反应达到平衡时,X的物质的量浓度为0.02mol?L-1 |
在20℃时,KCl的溶解度为34克.该温度时,25克水中加入10克KCl晶体,充分搅拌,所得溶液的溶质质量分数为( )
| A、40% | B、34% |
| C、28.6% | D、25.4% |
下列离子组能大量共存的是( )
| A、含有大量NH4+的溶液中:HCO3-、K+、Na+、Cl- |
| B、酚酞呈红色的溶液中:Na+、AlO2-、K+、HCO3- |
| C、含大量H+的溶液中:Na+、Cl-、NO3-、SO32- |
| D、加入Fe能放出H2的溶液中:Na+、K+、NO3-、SO42- |
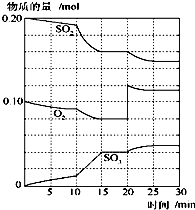 (1)在一定温度和压强下,有如下反应:2SO2(g)+O2(g) 2SO3(g),将1.6molSO2和0.8mol的O2放入一体积可变的密闭容器中,测得容器的起始容积为100L.经一段时间后,反应达到平衡,测得混合气体的密度为1.6g?L-1.请回答下列问题:
(1)在一定温度和压强下,有如下反应:2SO2(g)+O2(g) 2SO3(g),将1.6molSO2和0.8mol的O2放入一体积可变的密闭容器中,测得容器的起始容积为100L.经一段时间后,反应达到平衡,测得混合气体的密度为1.6g?L-1.请回答下列问题: