题目内容
9.运用元素周期律分析下面的推断,其中不正确的是( )| A. | 酸性:H2SiO3>H2CO3>H3PO4 | B. | 稳定性:PH3<H2S<HCl<HF | ||
| C. | 非金属性:Cl>S>P>Si | D. | 离子半径:Cl->F->Na+>Al3+ |
分析 A、元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B、元素的非金属性越强,对应的氢化物越稳定;
C、同周期元素从左到右元素的非金属性逐渐增强,同主族元素从上到下元素的非金属性逐渐减弱;
D、核外电子排布相同的离子,核电核数越大,离子半径越小,离子的电子层数越多,离子半径越大.
解答 解:A、非金属性:P>C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性:H3PO4>H2CO3>H2SiO3,故A错误;
B、非金属性:F>Cl>S>P,元素的非金属性越强,对应的氢化物越稳定,则氢化物的稳定性:HF>HCl>H2S>PH3,故B正确;
C、因同周期元素从左到右元素的非金属性逐渐增强,则有Cl>S>P>Si,故C正确;
D、核外电子排布相同的离子,核电核数越大,离子半径越小,所以F->Na+>Al3+,Cl-三个电子层,电子层数最多,离子的原子核外电子层数越多,半径越大,核外电子层数最小,则半径最小,则有Cl->F->Na+>Al3+,故D正确;
故选A.
点评 本题考查元素周期表与周期律的递变性,题目难度中等,学习中注重基础知识的积累.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
19.下列除杂方法不正确的是( )
| A. | 除去MgCl2溶液中的Fe3+,可向溶液中加入氨水调节pH | |
| B. | 除去污水中的金属离子Cu2+、Hg2+,可向溶液中加入FeS | |
| C. | 除去Cl2中混有的HCl,可以将气体通入饱和氯化钠溶液 | |
| D. | 除去CaCO3中的少量CaSO4,可以向其中加入足量饱和Na2CO3溶液后过滤 |
20.下列说法正确的是( )
| A. | H、N、Na、Fe、V五种元素中,有两种是第四周期元素 | |
| B. | 铁元素位于周期表中的第四周期,第8纵行,属于第ⅧA族 | |
| C. | 第四、五、六、七周期,每周期的元素共有18种 | |
| D. | 碱金属元素是指第ⅠA族的所有元素 |
17.下列物质中,属于芳香烃且属于苯的同系物的是( )
| A. |  | B. | 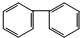 | C. | 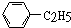 | D. |  |
4.下列物质中含离子键的是( )
| A. | 石英 | B. | 食盐 | C. | 干冰 | D. | 碘 |
14.已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是最内层电子数的3倍.下列说法不正确的是( )
| A. | 化合物YR4中各原子均满足8电子稳定结构 | |
| B. | 对应原子半径:Z<W<R | |
| C. | W与X、W与Y形成的化合物化学键类型完全相同 | |
| D. | Y的最高价氧化物对应的水化物是弱酸 |
1.下列元素位于第ⅥA族,且非金属性最强的元素是( )
| A. | F | B. | Cl | C. | O | D. | S |
18.下列各组物质中,化学键类型完全相同的是( )
| A. | HI和NaI | B. | H2S和CO2 | C. | Cl2和CCl4 | D. | Na2O2和NaOH |
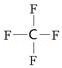
 ,1molO22+中含有的π键数目为2NA.
,1molO22+中含有的π键数目为2NA.