题目内容
17.下列物质中,属于芳香烃且属于苯的同系物的是( )| A. |  | B. | 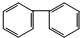 | C. | 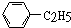 | D. |  |
分析 芳香烃通常指分子中含有苯环结构的碳氢化合物;
同系物指结构相似,在分子组成上相差一个或若干个CH2原子团的物质;
苯的同系物含有1个苯环,侧链为烷基,组成通式为CnH2n-6.
解答 解:A.是含有苯环结构的碳氢化合物,属于芳香烃,侧链是乙烯基,含有双键,不是烷基,不是苯的同系物,故A错误;
B.是含有苯环结构的碳氢化合物,属于芳香烃,分子中含有2个苯环,不相差若干个CH2原子团,不是苯的同系物,故B错误;
C.是含有苯环结构的碳氢化合物,属于芳香烃,侧链是乙基,分子组成比苯多2个CH2原子团,是苯的同系物,故C正确;
D.是含有苯环结构的碳氢化合物,属于芳香烃,分子中含有2个苯环,不相差若干个CH2原子团,不是苯的同系物,故D错误;
故选C.
点评 本题考查芳香烃、苯的同系物的概念、难度不大.要注意苯的同系物结构特点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列四位同学对“NH4Cl”的认识中,不正确的是( )
| A. | 甲同学认为氯化铵由N、H、Cl三种元素组成 | |
| B. | 乙同学认为一个氯化铵分子中含有一个NH4+和一个Cl- | |
| C. | 丙同学认为氯化铵由NH4+和Cl-构成 | |
| D. | 丁同学认为氯化铵中阴、阳离子个数比为1:1 |
12.下列各项不属于官能团的是( )
| A. | NO3- | B. | -Cl | C. | -CHO | D. | -NO2 |
2.被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为:Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A. | 该电池的正极为锌 | |
| B. | 电池正极反应式为:MnO2+e-+H2O═MnO(OH)+OH- | |
| C. | 该电池反应中二氧化锰起催化剂作用 | |
| D. | 当 0.l mol Zn 完全溶解时,流经电解液的电子数目为 1.204×l023 |
9.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 酸性:H2SiO3>H2CO3>H3PO4 | B. | 稳定性:PH3<H2S<HCl<HF | ||
| C. | 非金属性:Cl>S>P>Si | D. | 离子半径:Cl->F->Na+>Al3+ |
6.下表为元素周期表的一部分,根据表中所列出的元素回答下列问题
(1)最不活泼的元素是Ar(填元素符号),最活泼的非金属元素是F(填元素符号)
(2)可做半导体材料的元素是硅(填元素名称)
(3)氧离子结构示意图为 ,①、②、③原子半径从大到小的顺序是①②③
,①、②、③原子半径从大到小的顺序是①②③
(4)与水反应最剧烈的金属单质是Na(填元素符号),其反应的化学方程式是2Na+2H2O=2NaOH+H2↑
(5)既能与强酸又能与强碱反应的金属单质是Al(填元素符号)
(6)最高价氧化物的水化物中酸性最强的酸是HClO4写化学式)
(7)气态氢化物的稳定性:H2S<HCl(填“>”、“=”或“<”=;
(8)Al2O3中氧元素质量分数为47.1%.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)可做半导体材料的元素是硅(填元素名称)
(3)氧离子结构示意图为
 ,①、②、③原子半径从大到小的顺序是①②③
,①、②、③原子半径从大到小的顺序是①②③(4)与水反应最剧烈的金属单质是Na(填元素符号),其反应的化学方程式是2Na+2H2O=2NaOH+H2↑
(5)既能与强酸又能与强碱反应的金属单质是Al(填元素符号)
(6)最高价氧化物的水化物中酸性最强的酸是HClO4写化学式)
(7)气态氢化物的稳定性:H2S<HCl(填“>”、“=”或“<”=;
(8)Al2O3中氧元素质量分数为47.1%.
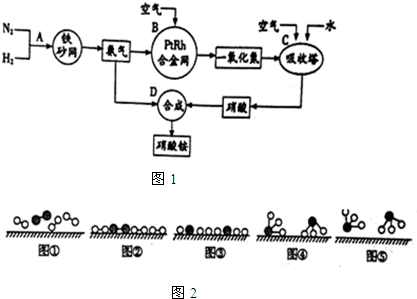
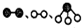 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.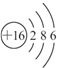 .
.