题目内容
19.下列除杂方法不正确的是( )| A. | 除去MgCl2溶液中的Fe3+,可向溶液中加入氨水调节pH | |
| B. | 除去污水中的金属离子Cu2+、Hg2+,可向溶液中加入FeS | |
| C. | 除去Cl2中混有的HCl,可以将气体通入饱和氯化钠溶液 | |
| D. | 除去CaCO3中的少量CaSO4,可以向其中加入足量饱和Na2CO3溶液后过滤 |
分析 A.加入氨水,除去铁离子,但引入新杂质铵根离子;
B.Cu2+、Hg2+加入FeS均发生沉淀的转化,生成更难溶的物质;
C.HCl极易溶于水,食盐水可抑制氯气的溶解;
D.向其中加入足量饱和Na2CO3溶液,Qc(CaCO3)>Ksp(CaCO3).
解答 解:A.除去MgCl2溶液中的Fe3+,可向溶液中加入MgO(或氢氧化镁等)调节pH,且不引入新杂质,故A错误;
B.Cu2+、Hg2+加入FeS均发生沉淀的转化,生成更难溶的物质CuS、HgS,能除去污水中的金属离子Cu2+、Hg2+,故B正确;
C.HCl极易溶于水,食盐水可抑制氯气的溶解,则将气体通入饱和氯化钠溶液可除杂,故C正确;
D.向其中加入足量饱和Na2CO3溶液,Qc(CaCO3)>Ksp(CaCO3),生成CaCO3,然后过滤,滤纸上的物质为CaCO3,故D正确;
故选A.
点评 本题考查物质的分离和提纯,为高考常见题型,侧重于学生的分析能力和实验能力的考查,题目难度不大,注意把握除杂的原则及反应原理的应用.

练习册系列答案
相关题目
14.已知:
(1)C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1
(3)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H3=-870.3kJ•mol-1
根据以上方程式可以计算出2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为( )
(1)C(s)+O2(g)═CO2(g)△H1=-393.5kJ•mol-1
(2)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1
(3)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H3=-870.3kJ•mol-1
根据以上方程式可以计算出2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为( )
| A. | +244.1 kJ•mol-1 | B. | -488.3 kJ•mol-1 | C. | -996.6 kJ•mol-1 | D. | +996.6 kJ•mol-1 |
4.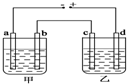 甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )
甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )
 甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )
甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )| A. | 甲槽中溶液是H2SO4,乙槽中溶液是NaOH | |
| B. | 甲槽中溶液是NaOH,乙槽中溶液是AgNO3 | |
| C. | 甲槽中溶液是AgNO3,乙槽中溶液是CuSO4 | |
| D. | 甲槽中溶液是CuSO4,乙槽中溶液是H2SO4 |
11.下列说法正确的是( )
①22.4L氧气中一定含有NA个氧分子
②将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是2mol/L
③18g水在标准状况下的体积为22.4L
④在常温常压下,20mLNH3和60mL氧气所含 分子数之比为1:3.
①22.4L氧气中一定含有NA个氧分子
②将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度是2mol/L
③18g水在标准状况下的体积为22.4L
④在常温常压下,20mLNH3和60mL氧气所含 分子数之比为1:3.
| A. | ①②③④ | B. | ①②④ | C. | ②③ | D. | ④ |
9.运用元素周期律分析下面的推断,其中不正确的是( )
| A. | 酸性:H2SiO3>H2CO3>H3PO4 | B. | 稳定性:PH3<H2S<HCl<HF | ||
| C. | 非金属性:Cl>S>P>Si | D. | 离子半径:Cl->F->Na+>Al3+ |
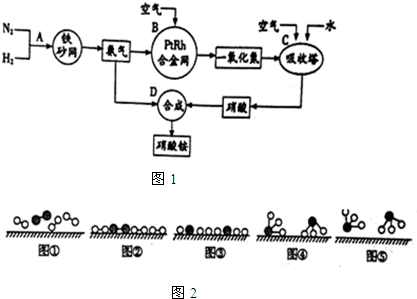
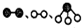 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.