题目内容
常温下A和B两种气体组成的混合物(A的式量大于B),经分析混合物气体中只含有C、O元素.
(1)当混合物中C、O的质量比总是小于3:8时,混合气体中A和B分别是 、 .
(2)当混合物中C、O的质量比总是介于3:8和3:4之间时,混合气体中A和B分别可能是 、 (填写化学式).
(1)当混合物中C、O的质量比总是小于3:8时,混合气体中A和B分别是
(2)当混合物中C、O的质量比总是介于3:8和3:4之间时,混合气体中A和B分别可能是
考点:有关混合物反应的计算
专题:计算题
分析:(1)根据已知条件,确定物质范围;根据氧的相对原子质量与碳的相对原子质量比,分别计算出CO2、O2和CO中氧,碳元素的质量比,再根据要求进行组合;
(2)根据(1)的分析可知混合气体为二氧化碳和一氧化碳.
(2)根据(1)的分析可知混合气体为二氧化碳和一氧化碳.
解答:
解:(1)由C、O元素组成的气体有:CO2、O2和CO,
氧的相对原子质量与碳的相对原子质量的比为:16:12=4:3,要使氧元素和碳元素的质量比等于8:3,氧原子与碳原子的个数比应为2:1;
CO2中C、O元素的质量比是12:36=3:8;
CO中C、O元素的质量比是12:16=3:4;
O2中C、O元素的质量比为无穷大;
如果不论以何种体积比混合,如果CO大量,明显不符合,所以符合条件的是CO2和O2的混合气体,
又因为A的相对分子质量大于B的相对分子质量,故A为二氧化碳,B为氧气,
故答案为:CO2;O2;
(2)当混合物中C、O的质量比总是介于3:8和3:4之间时,根据(1)的分析可知,混合气体为CO2、CO的混合物,
由于A的相对分子质量大于B的相对分子质量,则A为CO2,B为CO,
故答案为:CO2;CO.
氧的相对原子质量与碳的相对原子质量的比为:16:12=4:3,要使氧元素和碳元素的质量比等于8:3,氧原子与碳原子的个数比应为2:1;
CO2中C、O元素的质量比是12:36=3:8;
CO中C、O元素的质量比是12:16=3:4;
O2中C、O元素的质量比为无穷大;
如果不论以何种体积比混合,如果CO大量,明显不符合,所以符合条件的是CO2和O2的混合气体,
又因为A的相对分子质量大于B的相对分子质量,故A为二氧化碳,B为氧气,
故答案为:CO2;O2;
(2)当混合物中C、O的质量比总是介于3:8和3:4之间时,根据(1)的分析可知,混合气体为CO2、CO的混合物,
由于A的相对分子质量大于B的相对分子质量,则A为CO2,B为CO,
故答案为:CO2;CO.
点评:本题考查了混合物组成的计算,题目难度不大,正确分析CO2、O2和CO中C、O元素的含量为解答本题的关键,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
下列有关物质的分类正确的是( )
| A、CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
| B、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| C、CH2O2、C2H4O2、C3H6O2、C4H8O2属于同系物 |
| D、C60、C70、金刚石、石墨互为同素异形体 |
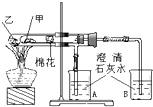 如图是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图实验装置、分析实验原理,并判断下列说法和做法,其中不科学的是( )
如图是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图实验装置、分析实验原理,并判断下列说法和做法,其中不科学的是( )| A、甲为小苏打,乙为纯碱 |
| B、整个实验过程中没有发现A烧杯的澄清石灰水变浑浊 |
| C、加热不久就能看到A烧杯的澄清石灰水变浑浊 |
| D、要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球 |
下列说法正确的是( )
| A、从2012年3月起公布了空气中的PM2.5:PM2.5是指空气中细颗粒物直径≤2.5 p m的颗粒物 |
| B、“可燃冰”的燃烧、从海水中提取镁、铜的电解精炼、石油分馏全都是化学变化的过程 |
| C、化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物 |
D、原子结构模型的演变历史可表示为: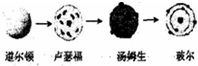 |
将10.6g由Mg、Al、Si组成的合金投入足量的NaOH溶液中,在标准状况下产生气体11.2L;另取等质量的合金溶于过量稀H2SO4中,合金质量减少了7.8g.则合金中Mg、Al、Si的物质的量之比为( )
| A、1:2:1 |
| B、2:1:1 |
| C、1:3:2 |
| D、1:1:2 |
下列物质排放到空气中,不会使空气受到污染的是( )
| A、煤燃烧时产生的烟气 |
| B、植物光合作用产生的气体 |
| C、石油化工工厂排放的废气 |
| D、汽车排放的尾气 |
取一定质量的CO和CO2的混合气体,通入足量Ba(OH)2溶液中,充分反应后过滤,发现生成的沉淀和所取的混合气体质量相等,则混合气体中,碳原子与氧原子的物质的量之比为( )
| A、181:209 | B、28:44 |
| C、1:2 | D、1:1 |