��Ŀ����
20��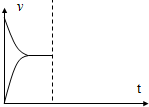 ��537�桢1.01��105Paʱ�����ݻ��ɱ���ܱ������г���1mol X��3mol Y����ʱ�ݻ�ΪV L�����ֺ��º�ѹ��������ӦX��g��+3Y��g��?2Z��g�����ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5��
��537�桢1.01��105Paʱ�����ݻ��ɱ���ܱ������г���1mol X��3mol Y����ʱ�ݻ�ΪV L�����ֺ��º�ѹ��������ӦX��g��+3Y��g��?2Z��g�����ﵽƽ��ʱ��ƽ����������Z���������Ϊ0.5����1���ﵽƽ��ʱ��X��ת����ԼΪ66.7%������Ӧ�ﵽƽ�����������������ʱ����ͨ��1mol X��3mol Y�Ļ�����壬������ͼ�л�������v�������棨v������Ӧ������ʱ��t�仯��ʾ��ͼ��
��2�����������¶Ⱥ�ѹǿ�㶨���䣬����������ֻ����4mol Z����Ӧ�ﵽƽ��ʱ��ƽ��������Y ���������Ϊ37.5%���������ݻ�Ϊ$\frac{4V}{3}$L��
��3������ѡһ�ݻ��̶�������ܱ��������Կ����¶Ȳ��䣬ʹ2mol X��6mol Y��Ӧ���ﵽƽ��ʱƽ��������Z�����������Ϊ0.5������ܱ��������ݻ�Ϊ$\frac{4V}{3}$��
��4�����¶���Ϊ537�棬�����������VL���䣨���ݣ��������г���a mol X��b mol Y��ʹ��Ӧ�ﵽƽ�⣬��ʱƽ��������Z�����������Ϊ0.5����ϵѹǿΪ1.01��105Pa����a��b=1��3����a=1.5mol��
���� ��ѹ�� X��g��+3Y��g��$\stackrel{\;}{?}$2Z��g����
��ʼ 1 3 0
ת�� x 3x 2x
ƽ��1-x 3-3x 2x
��ƽ��ʱ��ƽ����������Z���������Ϊ0.5��
��$\frac{2x}{4-2x}$=0.5�����x=$\frac{2}{3}$mol���Դ˽�ϵ�Чƽ���������⣮
��� �⣺��ѹ�� X��g��+3Y��g��$\stackrel{\;}{?}$2Z��g����
��ʼ 1 3 0
ת�� x 3x 2x
ƽ�� 1-x 3-3x 2x
��ƽ��ʱ��ƽ����������Z���������Ϊ0.5��
��$\frac{2x}{4-2x}$=0.5�����x=$\frac{2}{3}$mol��
��1��X��ת����ԼΪ$\frac{\frac{2}{3}mol}{1mol}$��100%=66.7%����������������ʱ����ͨ��1mol X��3mol Y�Ļ�����壬����ѹǿ���䣬�����ʲ��䣬ͼ��Ϊ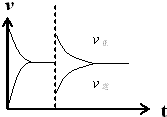 ��
��
�ʴ�Ϊ��66.7%�� ����
����
��2�����������¶Ⱥ�ѹǿ�㶨���䣬����������ֻ����4molZ��������ƽ���Ч����Y���������Ϊ$\frac{3-3��\frac{2}{3}}{4-2��\frac{2}{3}}$��100%=37.5%��
�����ʵ�������������ȿ�֪����ƽ������Ϊx����$\frac{4}{V}=\frac{\frac{8}{3}��2}{x}$�����x=$\frac{4V}{3}$L���ʴ�Ϊ��37.5%��$\frac{4V}{3}$��
��3���ݻ��̶�������ܱ��������Կ����¶Ȳ��䣬ʹ2mol X��6mol Y��Ӧ���ﵽƽ��ʱƽ��������Z�����������Ϊ0.5��
�����4molZ������ƽ���Ч�����Ϊ$\frac{4V}{3}$L���ʴ�Ϊ��$\frac{4V}{3}$��
��4�������������VL���䣨���ݣ��������г���a mol X��b mol Y��ʹ��Ӧ�ﵽƽ�⣬��ʱƽ��������Z�����������Ϊ0.5����ϵѹǿΪ1.01��105Pa����a��b=1��3���� X��g��+3Y��g��$\stackrel{\;}{?}$2Z��g����
��ʼ a 3a 0
ת�� x 3x 2x
ƽ��a-x 3a-3x 2x
��ƽ��ʱ��ƽ����������Z���������Ϊ0.5��
$\frac{2x}{4a-2x}$=0.5��4a-2x=4mol��
���a=1.5mol���ʴ�Ϊ��1.5mol��
���� ���⿼�黯ѧƽ��ļ��㼰��Чƽ�⣬Ϊ��Ƶ���㣬������ѧ���ķ��������������Ŀ��飬ע�⻯ѧƽ�����η��ļ��㼰��Чƽ�����������������ʵ����Ĺ�ϵ���ɽ����Ŀ�ѶȽϴ�

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д� ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�| A�� | ʹ�ô����ܼӿ췴Ӧ���� | |
| B�� | ѹǿ����Ӱ�컯ѧ��Ӧ���� | |
| C�� | �������µͣ���Ӧ���ʽ��ͣ�������Σ����С | |
| D�� | ����������������ı䣬���Դ˻�ѧ��Ӧ��������Ӱ�� |
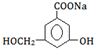
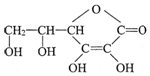 ������ʽΪC6H8O6�����е�-OH���ǻ�������������ƣ�����ά����C��Һ�е���������ɫ�ĺ��е��۵ĵ�ˮ���ɹ۲쵽����������ɫ��ȥ��˵��ά����C�л�ԭ�ԣ��������Ի�ԭ�ԣ���
������ʽΪC6H8O6�����е�-OH���ǻ�������������ƣ�����ά����C��Һ�е���������ɫ�ĺ��е��۵ĵ�ˮ���ɹ۲쵽����������ɫ��ȥ��˵��ά����C�л�ԭ�ԣ��������Ի�ԭ�ԣ���
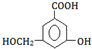
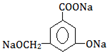 ��
��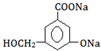 ��
�� ��
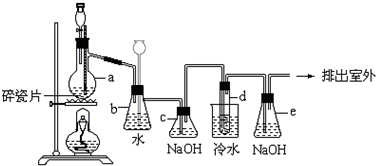
��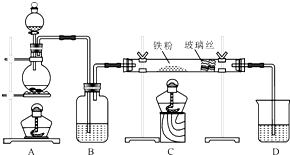 ��ҵ�ϣ���500�桫600�����м��ͨ������������ˮ�Ȼ�������֪������м���Ȼ��������Ȼ���������������ͼ��ʾ��װ��ģ���������̽������飮
��ҵ�ϣ���500�桫600�����м��ͨ������������ˮ�Ȼ�������֪������м���Ȼ��������Ȼ���������������ͼ��ʾ��װ��ģ���������̽������飮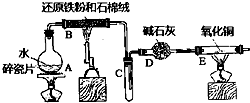 ijУ��ѧС��ѧ��������ͼ����װ�ý��С�����ˮ��Ӧ����ʵ�飬�������������й�ʵ�飮��ͼ�мгּ�β������װ�þ�����ȥ��
ijУ��ѧС��ѧ��������ͼ����װ�ý��С�����ˮ��Ӧ����ʵ�飬�������������й�ʵ�飮��ͼ�мгּ�β������װ�þ�����ȥ��