题目内容
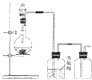
可用如图所示装置制取(必要时可加热)、净化、收集的气体是( )

| A、铜与稀硝酸反应制一氧化氮气体 |
| B、氯化铵与氢氧化钙固体反应制氨气 |
| C、锌和稀硫酸反应制氢气 |
| D、碳酸钠固体与硫酸反应制二氧化碳气体 |
考点:常见气体制备原理及装置选择
专题:实验题
分析:由装置图可知所制备的气体应为固液或液液制备,且能用浓硫酸干燥,并用向上排空气法收集,根据各选项中反应物的状态判断发生装置、气体的性质判断能否用浓硫酸干燥和能否用向上排空气法收集解答本题.
解答:
解:A、一氧化氮易于空气中氧气反应生成二氧化氮,不能用排空气法收集,只能用排水法收集,故A错误;
B、氯化铵与氢氧化钙都为固体,且反应需要加热,不能使用该发生装置,故B错误;
C、氢气密度比空气小,应用向下排空气法收集,故C错误;
D、二氧化碳为酸性气体,且不与浓硫酸反应,能用浓硫酸干燥,二氧化碳密度比空气大,用向上排空气法收集,故D正确;
故选D.
B、氯化铵与氢氧化钙都为固体,且反应需要加热,不能使用该发生装置,故B错误;
C、氢气密度比空气小,应用向下排空气法收集,故C错误;
D、二氧化碳为酸性气体,且不与浓硫酸反应,能用浓硫酸干燥,二氧化碳密度比空气大,用向上排空气法收集,故D正确;
故选D.
点评:本题考查常见气体的制备和收集,注意从实验装置图判断气体所具备的性质,以选择适合的气体,本题难度不大.

练习册系列答案
相关题目
研究二氧化碳性质的微型实验装置如图,现用70%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气.下列说法中错误的是( )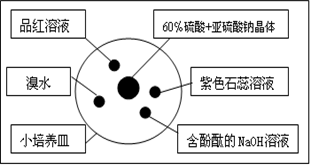

| A、溴水橙色褪去,原因是SO2气体具有漂白性 |
| B、含酚酞的NaOH溶液红色变浅,原因是SO2气体具有漂白性 |
| C、品红溶液褪色,原因是SO2气体具有漂白性 |
| D、紫色石蕊溶液变蓝色,原因是SO2气体具有酸性和漂白性 |
化工生产中常用的CO和H2,可通过烃与水蒸气反应得到.其中甲烷可发生以下两个反应:
(1)CH4(g)+
O2(g)=2H2(g)+CO(g);△H=-36kJ/mol
(2)CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+216kJ/mol
下列化学反应方程式中,反应热为零的是( )
(1)CH4(g)+
| 1 |
| 2 |
(2)CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+216kJ/mol
下列化学反应方程式中,反应热为零的是( )
| A、7CH4(g)+3O2(g)+H2O(g)=7CO(g)+15H2(g) |
| B、5CH4(g)+2O2(g)+H2O(g)=5CO(g)+11H2(g) |
| C、4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g) |
| D、3CH4(g)+O2(g)+H2O(g)=3CO(g)+7H2(g) |
下列有关银镜反应实验的说法中不正确的是( )
| A、实验前试管先用热的烧碱溶液洗涤,再用蒸馏水洗涤 |
| B、向2%的硝酸银溶液中滴入2%的稀氨水液直到生成的沉淀恰好溶解为止 |
| C、可采用水浴加热,也可直接加热 |
| D、可用稀硝酸洗去试管内的银镜 |
 金银花是治疗和预防甲型 H1N1的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式如图所示,下列有关绿原酸的说法不正确的是( )
金银花是治疗和预防甲型 H1N1的常见中草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式如图所示,下列有关绿原酸的说法不正确的是( )| A、分子式为C16H18O9 |
| B、1 mol绿原酸与溴水反应最多消耗4molBr2 |
| C、1 mol绿原酸最多与5 mol H2加成 |
| D、1 mol绿原酸最多与4 mol NaOH反应 |
 某同学设计了一种电解法制取Fe(OH)2的实验装置,如图所示通电后,B极表面有气泡产生,且溶液中产生大量的白色沉淀,较长时间不变色,下列说法正确的是.
某同学设计了一种电解法制取Fe(OH)2的实验装置,如图所示通电后,B极表面有气泡产生,且溶液中产生大量的白色沉淀,较长时间不变色,下列说法正确的是.| A、电源a是负极 |
| B、电解质溶液一定是NaOH溶液 |
| C、A、B两端都必须用铁做电极 |
| D、B极附近溶液pH增大 |
将一小粒金属投入盛有水的小烧杯中,实验现象描述不合理的是( )
| A、金属钠块浮于液面上,四处游动 |
| B、金属钠熔化成液态小球 |
| C、烧杯内溶液颜色逐渐变红 |
| D、听到(可燃性气体)轻微的爆鸣声 |
 雾.试完成下列问题:
雾.试完成下列问题: