题目内容
甲同学用如图所示的装置制取氯化铁,A是氯气发生装置(用浓盐酸和二氧化锰),B中的饱和食盐水用来除氯气中混有的氯化氢.D管中放置有铁粉,氯化铁在潮湿的空气中会和水剧烈反应冒出烟 雾.试完成下列问题:
雾.试完成下列问题:
(1)烧瓶A中发生反应的离子方程式为 .
(2)气体通过容器C的目的是
(3)石英玻璃管D中发生反应的化学方程式是
(4)球形干燥管E中碱石灰的作用是
(5)氯化铁在潮湿的空气中和水剧烈反应冒出烟雾的化学方程式是
(6)乙同学认为甲同学装置中的B可以不用,将A与C直接相连就行了.
丙同学认为乙同学这样做,可能引起爆炸,而且生成的氯化铁中可能混有氯化亚铁.丙同学为了验证自己的猜想是正确的,取了乙同学制取的氧化铁固体少量加入试管中,并加入稀硝酸,观察到液面上面出现红棕色,而且红棕色渐渐上移,最后只在试管口可观察到红棕色,试管内气体无色.由此丙同学认为乙同学制取的氯化铁固体中含有氯化亚铁.
你认为丙同学所说的爆炸可能原因是 ;你认为丙同学用稀硝酸而不用酸性高锰酸钾溶液来检验氯化亚铁的存在的原因是 .
 雾.试完成下列问题:
雾.试完成下列问题:(1)烧瓶A中发生反应的离子方程式为
(2)气体通过容器C的目的是
(3)石英玻璃管D中发生反应的化学方程式是
(4)球形干燥管E中碱石灰的作用是
(5)氯化铁在潮湿的空气中和水剧烈反应冒出烟雾的化学方程式是
(6)乙同学认为甲同学装置中的B可以不用,将A与C直接相连就行了.
丙同学认为乙同学这样做,可能引起爆炸,而且生成的氯化铁中可能混有氯化亚铁.丙同学为了验证自己的猜想是正确的,取了乙同学制取的氧化铁固体少量加入试管中,并加入稀硝酸,观察到液面上面出现红棕色,而且红棕色渐渐上移,最后只在试管口可观察到红棕色,试管内气体无色.由此丙同学认为乙同学制取的氯化铁固体中含有氯化亚铁.
你认为丙同学所说的爆炸可能原因是
考点:性质实验方案的设计
专题:实验设计题
分析:由实验的目的和反应的原理可知,实验室用第一个装置A制备氯气,气体分别通入盛有饱和食盐水的洗气瓶和盛有浓硫酸的洗气瓶,除杂干燥后进入D装置与铁粉反应制取氯化铁,氯气有毒,不能直接排放到空气中,加装盛放碱石灰的装置E吸收,同时防止空气中水蒸气进入装置D中.
(1)实验室是用二氧化锰和浓盐酸反应制氯气,反应生成氯气、二氯化锰、水,依据离子方程式书写方法,易溶于水的强电解质拆成离子;
(2)氯化铁在潮湿的空气中会和水剧烈反应冒出烟雾,装置C用来干燥氯气;
(3)铁与氯气反应生成氯化铁;
(4)E吸收剩余的氯气,同时防止空气中水蒸气进入装置D中;
(5)氯化铁在潮湿的空气中和水剧烈反应冒出烟雾是氯化铁水解生成HCl;
(6)若不加B装置,生成的HCl气体可以与铁反应生成氢气,在加热时有可能发生爆炸,氯离子具有还原性,能够使高锰酸钾溶液褪色.
(1)实验室是用二氧化锰和浓盐酸反应制氯气,反应生成氯气、二氯化锰、水,依据离子方程式书写方法,易溶于水的强电解质拆成离子;
(2)氯化铁在潮湿的空气中会和水剧烈反应冒出烟雾,装置C用来干燥氯气;
(3)铁与氯气反应生成氯化铁;
(4)E吸收剩余的氯气,同时防止空气中水蒸气进入装置D中;
(5)氯化铁在潮湿的空气中和水剧烈反应冒出烟雾是氯化铁水解生成HCl;
(6)若不加B装置,生成的HCl气体可以与铁反应生成氢气,在加热时有可能发生爆炸,氯离子具有还原性,能够使高锰酸钾溶液褪色.
解答:
解:由据实验的目的和反应的原理可知,实验室用第一个装置A制备氯气,气体分别通入盛有饱和食盐水的洗气瓶和盛有浓硫酸的洗气瓶,除杂干燥后进入D装置与铁粉反应制取氯化铁,氯气有毒,不能直接排放到空气中,加装盛放碱石灰的装置E吸收,同时防止空气中水蒸气进入装置D中,
(1)实验室是用二氧化锰和浓盐酸反应制氯气,反应生成氯气、二氯化锰、水,反应的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(2)装置C用来干燥氯气,防止水蒸气进入装置D中,故答案为:干燥氯气;
(3)铁与氯气反应生成氯化铁,反应方程式为2Fe+3Cl2
2FeCl3,故答案为:2Fe+3Cl2
2FeCl3;
(4)氯气有毒,不能直接排放到空气中,加装盛放碱石灰的装置E吸收,同时防止空气中水蒸气进入装置D中,故答案为:吸收剩余氯气,防止空气中水蒸气进入装置D中;
(5)氯化铁在潮湿的空气中和水剧烈反应冒出烟雾是氯化铁水解生成HCl,水解方程式为FeCl3+3H2O Fe(OH)3+3HCl,
Fe(OH)3+3HCl,
故答案为:FeCl3+3H2O Fe(OH)3+3HCl;
Fe(OH)3+3HCl;
(6)若不加B装置,生成的HCl气体可以与铁反应生成氢气,在加热时有可能发生爆炸,氯离子具有还原性,能够使高锰酸钾溶液褪色,故答案为:氯化氢和铁反应生成的氢气与氯气混合加热引起爆炸;氯离子也能使酸性高锰酸钾溶液褪色.
(1)实验室是用二氧化锰和浓盐酸反应制氯气,反应生成氯气、二氯化锰、水,反应的离子方程式为:MnO2+4H++2Cl-
| ||
故答案为:MnO2+4H++2Cl-
| ||
(2)装置C用来干燥氯气,防止水蒸气进入装置D中,故答案为:干燥氯气;
(3)铁与氯气反应生成氯化铁,反应方程式为2Fe+3Cl2
| ||
| ||
(4)氯气有毒,不能直接排放到空气中,加装盛放碱石灰的装置E吸收,同时防止空气中水蒸气进入装置D中,故答案为:吸收剩余氯气,防止空气中水蒸气进入装置D中;
(5)氯化铁在潮湿的空气中和水剧烈反应冒出烟雾是氯化铁水解生成HCl,水解方程式为FeCl3+3H2O
 Fe(OH)3+3HCl,
Fe(OH)3+3HCl,故答案为:FeCl3+3H2O
 Fe(OH)3+3HCl;
Fe(OH)3+3HCl;(6)若不加B装置,生成的HCl气体可以与铁反应生成氢气,在加热时有可能发生爆炸,氯离子具有还原性,能够使高锰酸钾溶液褪色,故答案为:氯化氢和铁反应生成的氢气与氯气混合加热引起爆炸;氯离子也能使酸性高锰酸钾溶液褪色.
点评:本题考查了制取氯气实验相关内容的探究,注意实验室制备气体的实验装置和反应原理,把握物质的主要性质,注重基础知识的积累,题目难度中等.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
将8.7g MnO2粉末与含14.6gHCl的浓盐酸共热,完全反应后,生成的氯气体积(标准状况)( )
| A、等于4.48L |
| B、等于2.24L |
| C、介于2.24~4.48L |
| D、小于2.24L |
以下实验能获得成功的是( )
| A、用酸性KMnO4溶液鉴别乙烯和丙烯 |
| B、将铁屑、溴水、苯混合制溴苯 |
| C、碳酸氢钠溶液中滴入苯酚的水溶液后会放出二氧化碳 |
| D、将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
可用如图所示装置制取(必要时可加热)、净化、收集的气体是( )
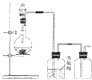

| A、铜与稀硝酸反应制一氧化氮气体 |
| B、氯化铵与氢氧化钙固体反应制氨气 |
| C、锌和稀硫酸反应制氢气 |
| D、碳酸钠固体与硫酸反应制二氧化碳气体 |
若液氨相当于地球上的水,它可满足本星上生物生存的需要,那么木星上生物体内与地球上生物体内葡萄糖的分子结构相当的化合物是( )
| A、CH2NH2-(CHNH2)4CH=NH |
| B、CH2NH3-(CHNH2)4CHO |
| C、CH2OH-(CHOH)4 CHO |
| D、CH2OH-(CHOH)4 CH=NH |
 金银花是治疗和预防甲型HINI的常见草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式如图,下列有关绿原酸的说法不正确的是:( )
金银花是治疗和预防甲型HINI的常见草药,有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构式如图,下列有关绿原酸的说法不正确的是:( )| A、分子式为C16H18O9 |
| B、1mol绿原酸与溴水反应最多消耗4mol Br2 |
| C、1mol绿原酸最多与 5molH2加成 |
| D、1mol 绿原酸最多与4mol NaOH反应 |
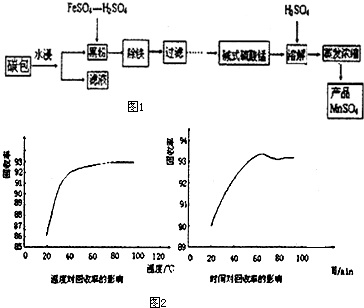
 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.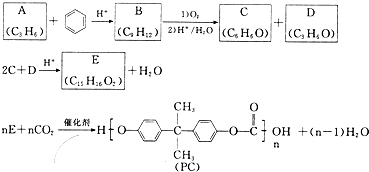 PC是一种可降解的聚碳酸酯类高分子材料,由于具有优良的耐冲击性和韧性,因而得到了广泛的应用.如图是某研究小组开发的生产PC的合成路线:
PC是一种可降解的聚碳酸酯类高分子材料,由于具有优良的耐冲击性和韧性,因而得到了广泛的应用.如图是某研究小组开发的生产PC的合成路线: