题目内容
化工生产中常用的CO和H2,可通过烃与水蒸气反应得到.其中甲烷可发生以下两个反应:
(1)CH4(g)+
O2(g)=2H2(g)+CO(g);△H=-36kJ/mol
(2)CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+216kJ/mol
下列化学反应方程式中,反应热为零的是( )
(1)CH4(g)+
| 1 |
| 2 |
(2)CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+216kJ/mol
下列化学反应方程式中,反应热为零的是( )
| A、7CH4(g)+3O2(g)+H2O(g)=7CO(g)+15H2(g) |
| B、5CH4(g)+2O2(g)+H2O(g)=5CO(g)+11H2(g) |
| C、4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g) |
| D、3CH4(g)+O2(g)+H2O(g)=3CO(g)+7H2(g) |
考点:有关反应热的计算
专题:
分析:已知(1)CH4(g)+
O2(g)=2H2(g)+CO(g);△H=-36kJ/mol,(2)CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+216kJ/mol,根据选项中的目标方程式,转化方程式(1)和(2)通过盖斯定律计算.
| 1 |
| 2 |
解答:
解:A.(1)×6+(2)得7CH4(g)+3O2(g)+H2O(g)=7CO(g)+15H2(g)△H=(-36kJ/mol)×6+216kJ/mol=0kJ/mol,故A选;
B.(1)×4+(2)得4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g)△H=(-36kJ/mol)×4+(216kJ/mol)=+72kJ/mol,故B不选;
C.(1)×2+(2)×2得4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g)△H=(-36kJ/mol)×2+(216kJ/mol)×2=+360kJ/mol,故C不选;
D.(1)×2+(2)得4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g)△H=(-36kJ/mol)×2+(216kJ/mol)=+144kJ/mol,故D不选.
故选A.
B.(1)×4+(2)得4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g)△H=(-36kJ/mol)×4+(216kJ/mol)=+72kJ/mol,故B不选;
C.(1)×2+(2)×2得4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g)△H=(-36kJ/mol)×2+(216kJ/mol)×2=+360kJ/mol,故C不选;
D.(1)×2+(2)得4CH4(g)+O2(g)+2H2O(g)=4CO(g)+10H2(g)△H=(-36kJ/mol)×2+(216kJ/mol)=+144kJ/mol,故D不选.
故选A.
点评:本题考查了盖斯定律的应用,侧重于计算能力的考查,题目难度中等,注意把握盖斯定律的含义和使用方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
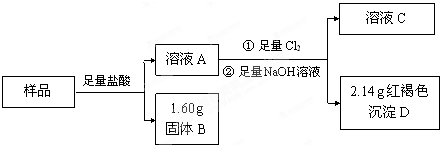
将8.7g MnO2粉末与含14.6gHCl的浓盐酸共热,完全反应后,生成的氯气体积(标准状况)( )
| A、等于4.48L |
| B、等于2.24L |
| C、介于2.24~4.48L |
| D、小于2.24L |
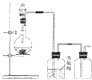
可用如图所示装置制取(必要时可加热)、净化、收集的气体是( )

| A、铜与稀硝酸反应制一氧化氮气体 |
| B、氯化铵与氢氧化钙固体反应制氨气 |
| C、锌和稀硫酸反应制氢气 |
| D、碳酸钠固体与硫酸反应制二氧化碳气体 |
下列实验现象中,由于发生取代反应而引起的是( )
| A、乙烯通入溴的四氯化碳溶液中,溶液褪色 |
| B、苯滴加到溴水中,振荡后水层接近无色 |
| C、甲烷和氯气的混合气体在光照后,瓶壁上有油状液滴附着 |
| D、将灼热的铜丝迅速插入乙醇中,反复多次,有刺激性气味产生 |
 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.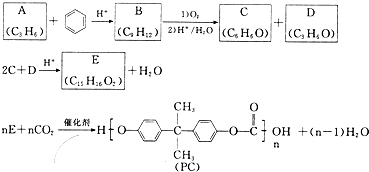 PC是一种可降解的聚碳酸酯类高分子材料,由于具有优良的耐冲击性和韧性,因而得到了广泛的应用.如图是某研究小组开发的生产PC的合成路线:
PC是一种可降解的聚碳酸酯类高分子材料,由于具有优良的耐冲击性和韧性,因而得到了广泛的应用.如图是某研究小组开发的生产PC的合成路线: