题目内容
16.制取水处理剂ClO2的化学方程式为:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )| A. | KClO3在反应中得到电子 | |
| B. | ClO2是还原产物 | |
| C. | H2C2O4在反应中被还原 | |
| D. | 1molKClO3参加反应有1mol电子转移 |
分析 2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O中,Cl元素的化合价降低,C元素的化合价升高,以此来解答.
解答 解:A.反应中Cl元素由+5价降低为+4价,则KClO3为氧化剂,在反应中得到电子,故A正确;
B.因KClO3为氧化剂,在反应中被还原,则ClO2是还原产物,故B正确;
C.反应中碳元素的化合价由+3价升高到+4价,则H2C2O4为还原剂,在反应中被氧化,故C错误;
D.反应中Cl元素由+5价降低为+4价,1molKClO3参加反应有1mol×(5-4)=1mol电子转移,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意化合价的判断,题目难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
6.饮用水的消毒剂有多种,其中杀菌能力强且不会影响水质的理想消毒剂是( )
| A. | 臭氧 | B. | 漂白粉 | C. | 液氯 | D. | 明矾 |
4.常温下能在浓HNO3中溶解的金属是( )
| A. | Al | B. | Fe | C. | .Pt | D. | Cu |
11.2mol甲烷完全和氯气发生取代反应,生成四种取代产物的物质的量相同,则消耗氯气的物质的量为( )
| A. | 5mol | B. | 4mol | C. | 6mol | D. | 3.5mol |
1.A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示.
A是短周期中原子半径最小的元素,B、C二种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素.下列说法错误的是( )
| B | C |
| D |
| A. | 简单离子的半径大小关系:C>E | |
| B. | D元素的气态氢化物比C元素的气态氢化物稳定 | |
| C. | 由B、E可组成离子化合物,阴、阳离子个数比为1:1或1:2 | |
| D. | 由C、D、E中的二种元素组成的化合物,溶液显中性或碱性 |
8.下列叙述中,不正确的是( )
| A. | C5H12的同分异构体中,其中的一种只能生成一种一氯代物 | |
| B. | CH3-CH﹦CH-C≡C-CF3分子结构中6个碳原子不可能都在同一平面上 | |
| C. | 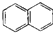 不属于脂环化合物 不属于脂环化合物 | |
| D. | 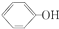 和 和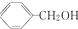 不是同系物 不是同系物 |
6.下列各项中表达正确的是( )
| A. | 小苏打的化学式:NaHCO3 | |
| B. | 镁离子的结构示意图: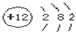 | |
| C. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| D. | NaOH的电离方程式:NaOH=Na++O2-+H+ |
 ,在周期表中的位置第四周期ⅢB族,属于d区.
,在周期表中的位置第四周期ⅢB族,属于d区.