题目内容
6.下列各项中表达正确的是( )| A. | 小苏打的化学式:NaHCO3 | |
| B. | 镁离子的结构示意图: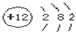 | |
| C. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| D. | NaOH的电离方程式:NaOH=Na++O2-+H+ |
分析 A.小苏打为碳酸氢钠的俗名;
B.镁离子的核外电子总数为10,最外层达到8电子稳定结构;
C.元素符号的左上角为质量数、左下角为质子数;
D.氢氧化钠在溶液中电离出钠离子和氢氧根离子.
解答 解:A.碳酸氢钠的俗名为小苏打,化学式为:NaHCO3,故A正确;
B.镁离子的核电荷数为12,核外电子总数为10,镁离子正确的结构示意图为: ,故B错误;
,故B错误;
C.质量数为37的氯原子的正确表示方法为:1737Cl,故C错误;
D.NaOH为强电解质,在溶液中完全电离出钠离子和氢氧根离子,其正确的电离方程式为:NaOH=Na++OH-,故D错误;
故选A.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及化学式、离子结构示意图、元素符号、电离方程式等掌握,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
16.制取水处理剂ClO2的化学方程式为:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )
| A. | KClO3在反应中得到电子 | |
| B. | ClO2是还原产物 | |
| C. | H2C2O4在反应中被还原 | |
| D. | 1molKClO3参加反应有1mol电子转移 |
17.高铁酸钾(K2FeO4)为新型净水剂,可溶于水.工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O、②Na2FeO4+2KOH═K2FeO4+2NaOH下列说法不正确的是( )
| A. | Na2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 | |
| B. | 反应①中,NaCl是氧化产物 | |
| C. | 反应①为氧化还原反应,反应②为复分解反应 | |
| D. | 若有2mol FeCl3发生反应,转移电子的物质的量为6mol |
14.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下11.2L的水中含有0.5个NA水分子 | |
| B. | 0.1mol•L-1 NaCl溶液中Na+的数目为0.1NA | |
| C. | 1mol H2和O2的混合气体中含NA个分子 | |
| D. | 在常温常压下,18克水含有的原子数为3NA |
1.某元素的原子结构示意图为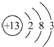 ,下列关于该元素的说法中,错误的是( )
,下列关于该元素的说法中,错误的是( )
 ,下列关于该元素的说法中,错误的是( )
,下列关于该元素的说法中,错误的是( )| A. | 它是一种金属元素 | B. | 它的阳离子有10个质子 | ||
| C. | 它的阳离子带3个单位正电荷 | D. | 其原子核外有13个电子 |
11.下列关于甲烷的叙述错误的是( )
| A. | 天然气的主要成分 | |
| B. | 最简单的有机物 | |
| C. | 二氯取代物有两种结构 | |
| D. | 与氯气在光照条件下能发生取代反应 |
18.下列有关有机物结构的叙述不正确的是( )
| A. | 一氟一氯甲烷只有一种结构,可以证明甲烷是正四面体结构而不是平面正方形结构 | |
| B. | 乙烯和甲苯分子中所有原子都在同一个平面上 | |
| C. | 邻二甲苯没有同分异构体表明苯的凯库勒结构式存在局限,不准确 | |
| D. | 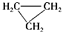 和CH3-CH═CH2互为同分异构体 和CH3-CH═CH2互为同分异构体 |
15.下列有关说法正确的是( )
| A. | 相同温度下,0.1 mol•L-1NH4Cl溶液比0.1 mol•L-1NH4HSO4溶液含有的[NH4+]更大 | |
| B. | 将0.1 mol•L-1硫酸溶液从常温加热至100℃,溶液的pH保持不变 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ | |
| D. | 在蒸发皿中加热蒸发(低于400℃)FeCl3溶液,可以得到FeCl3固体 |
1.下列化学用语表示正确的是( )
| A. | 水的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| B. | 乙烷的结构简式:C2H6 | |
| C. | 铝的原子结构示意图: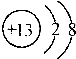 | |
| D. | 硫酸钠的电离方程式:Na2SO4═2Na++SO42- |