题目内容
将一定量下列溶液混合后加热蒸干并灼烧,所得固体不可能为纯净物的是( )
| A、FeCl3与FeCl2 |
| B、KHCO3与KOH |
| C、NH4Cl与NaCl |
| D、AlCl3与Al2(SO4)3 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:A.亚铁离子被氧化生成铁离子,氯化氢易挥发,蒸干灼烧最终得到氧化铁固体;
B.碳酸氢钾受热易分解生成碳酸钾,氢氧化钾和二氧化碳反应生成碳酸钾,蒸干灼烧最终得到碳酸钾;
C.氯化铵受热分解生成氯化氢和氨气,蒸干灼烧最终得到氯化钠;
D.氯化铝溶液蒸干灼烧最终得到氧化铝,硫酸铝溶液蒸干灼烧最终得到硫酸铝.
B.碳酸氢钾受热易分解生成碳酸钾,氢氧化钾和二氧化碳反应生成碳酸钾,蒸干灼烧最终得到碳酸钾;
C.氯化铵受热分解生成氯化氢和氨气,蒸干灼烧最终得到氯化钠;
D.氯化铝溶液蒸干灼烧最终得到氧化铝,硫酸铝溶液蒸干灼烧最终得到硫酸铝.
解答:
解:A.氯化铁和氯化亚铁的混合液,加热促进氯化铁和氯化亚铁水解,亚铁离子不稳定易被氧化为铁离子,蒸干过程中促进氯化氢挥发,蒸干最终得到氢氧化铁固体,再灼烧时氢氧化铁分解生成氧化铁,所以得到的固体是纯净物,故A不选;
B.二者反应生成碳酸钾和水,如果碳酸氢钾过量,在灼烧时碳酸氢钾分解生成碳酸钾,如果氢氧化钾过量,在加热过程中生成碳酸钾,所以最终得到的固体是碳酸钾,为纯净物,故B不选;
C.蒸干灼烧过程中氯化铵分解生成氨气和氯化氢,所以最终得到的固体是氯化钠,为纯净物,故C不选;
D.氯化铝水解生成氢氧化铝和氯化氢,氯化氢易挥发,氢氧化铝分解生成氧化铝,所以蒸干灼烧氯化铝溶液最终得到氧化铝固体,硫酸铝易水解,但硫酸不挥发且不分解,所以最终得到的固体是硫酸铝,则蒸干灼烧二者的混合溶液时得到的固体是氧化铝和硫酸铝,故D选;
故选D.
B.二者反应生成碳酸钾和水,如果碳酸氢钾过量,在灼烧时碳酸氢钾分解生成碳酸钾,如果氢氧化钾过量,在加热过程中生成碳酸钾,所以最终得到的固体是碳酸钾,为纯净物,故B不选;
C.蒸干灼烧过程中氯化铵分解生成氨气和氯化氢,所以最终得到的固体是氯化钠,为纯净物,故C不选;
D.氯化铝水解生成氢氧化铝和氯化氢,氯化氢易挥发,氢氧化铝分解生成氧化铝,所以蒸干灼烧氯化铝溶液最终得到氧化铝固体,硫酸铝易水解,但硫酸不挥发且不分解,所以最终得到的固体是硫酸铝,则蒸干灼烧二者的混合溶液时得到的固体是氧化铝和硫酸铝,故D选;
故选D.
点评:本题考查了盐类水解,明确物质的性质是解本题关键,根据物质发生的反应来分析解答即可,注意A中亚铁离子易被氧化,D中硫酸没有挥发性,注意加热蒸干灼烧硫酸铝和氯化铝或硝酸铝的区别,题目难度中等.

练习册系列答案
相关题目
下列性质的递变中,正确的是( )
| A、O、S、Na的原子半径依次增大 |
| B、LiOH、KOH、CsOH的碱性依次增强 |
| C、HF、NH3、SiH4的稳定性依次增强 |
| D、HCl、HBr、HI的还原性依次减弱 |
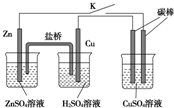 用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )| A、铜棒为正极,其电极反应式为:2H++2e-═H2↑ |
| B、烧杯右侧碳棒为阴极,其电极表面有红色物质析出 |
| C、反应中消耗锌的质量为13g |
| D、导线中通过电子的物质的量为0.2 mol |
下列电离方程式书写正确的是( )
| A、NaHCO3=Na++H++CO32- |
| B、HF?H++F- |
| C、H2CO3?2H++CO32- |
| D、CH3COONH4?CH3COO-+NH4+ |
下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A、1mol苯乙烯( )中含有的C=C数为4NA )中含有的C=C数为4NA |
| B、标准状况下,2.24L溴乙烷含有的分子数为0.1NA |
| C、某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA |
| D、1mol甲基含10NA个电子 |
根据表中烃的含氧衍生物分子式排列规律,空格中烃的含氧衍生物的有关判断正确的是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH2O2 | C2H4O | C3H6O2 | C4H8O | C6H12O | C7H14O2 | C8H16O |
| A、能与NaHCO3反应的同分异构体有3种 |
| B、该物质肯定能发生加成反应和取代反应 |
| C、1mol符合该分子式的一种有机物与足量Na反应能生成1mol H2,则该物质中一定存在一条碳碳双键 |
| D、该物质与丁烷以任意物质的量比混合时,只要混合物的物质的量一定,消耗的氧气量也一定 |
太阳能电池板面对太阳时,一部分电能直接供给“天宫一号”,一部分电能则储存在电池里,供背离太阳时使用.“天宫一号”使用的是镍氢电池,电解质溶液显碱性.其反应方程式为:LaNi5+Ni(OH)2
LaNi5H+NiOOH.下列有关说法不正确的是( )
| 放电 |
| 充电 |
| A、放电时镍被还原 |
| B、放电时负极LaNi5H+OH--e-═LaNi5+H2O |
| C、充电时OH-向阴极移动 |
| D、充电时每消耗1mol Ni(OH)2转移1mol电子 |
下列各组物质中互称为同分异构体的是( )
| A、乙醇(CH3CH2OH)与二甲醚(CH3OCH3) |
| B、水与重水 |
| C、红磷与白磷 |
| D、O2与O3 |