题目内容
14.下列物质晶体结构中含有正四面体结构的化合物是( )| A. | SiO2 | B. | 金刚石 | C. | KCl | D. | 干冰 |
分析 具有正四面体结构的物质中,中心原子价层电子对个数是4,且不含孤电子对,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.
解答 解:A.SiO2晶体结构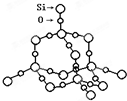 ,二氧化硅晶体中存在正四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,Si处于中心,O处于4个顶角,故A正确;
,二氧化硅晶体中存在正四面体结构单元,每个硅原子能构成四个共价键,每个氧原子能形成2个共价键,Si处于中心,O处于4个顶角,故A正确;
B.金刚石的结构为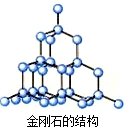 ,每个碳原子和四个碳原子形成共价键,所以其价层电子对个数是4,为正四面体结构,但金刚石为单质,故B错误;
,每个碳原子和四个碳原子形成共价键,所以其价层电子对个数是4,为正四面体结构,但金刚石为单质,故B错误;
C.KCl是体心立方晶体结构,晶体结构中不含有正四面体结构,故C错误;
D.二氧化碳分子中碳原子价层电子对个数=2+$\frac{1}{2}$(4-2×2)=2,所以分子为直线形分子,结构为O=C=O,故D错误;
故选A.
点评 本题考查了微粒空间构型的判断,根据价层电子对互斥理论来分析解答,注意金刚石结构,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列说法正确的是( )
| A. | 原子半径大小:Ca>S | B. | 金属性强弱:Na<Mg | ||
| C. | 酸性强弱:HBrO4>HClO4 | D. | 碱性强弱:NaOH>KOH |
5.下列各对物质中互为同系物的是( )
| A. | CH≡CH和CH2═CH-CH═CH2 | B. | CH3-CH═CH2和CH3-CH2-CH═CH2 | ||
| C. | CH3-CH3和CH3-CH═CH2 | D. | 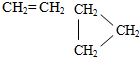 |
2.某有机物结构简式如图,下列说法错误的是( )


| A. | 该有机物属于饱和链烃 | |
| B. | 该有机物可由两种单炔烃分别与氢气加成得到 | |
| C. | 该烃与2,3-二甲基丁烷互为同系物 | |
| D. | 该烃的一氯取代产物共有5种 |
6.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 过氧化氢分解制得标准状况下1.12 L O2,转移电子数目为 0.2 NA | |
| B. | 足量铜与含硝酸4 mol 的浓硝酸反应,生成氮的氧化物中氮的化合价为+4 价 | |
| C. | 1 mol 铜与足量浓硝酸反应,生成标况下气体体积为44.8 L | |
| D. | 一定温度下,1 L 0.50 mol•L-1 NH4NO3溶液中含氮原子个数为NA |
3.下列关于苯的叙述正确的是( )
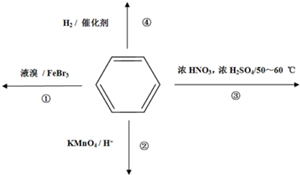

| A. | 反应①为取代反应,有机产物与水混合浮在上层 | |
| B. | 反应②为氧化反应,反应现象是火焰为淡蓝色 | |
| C. | 反应③为取代反应,有机产物是一种烃的衍生物 | |
| D. | 反应④中1 mol苯最多与6 mol H2发生加成反应 |

