题目内容
9.家用液化气的主要成分之一是丁烷,当10g丁烷完全燃烧并生成CO2和液态水时,放出的热量为500kJ.试写出丁烷燃烧的热化学方程式:C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol.分析 根据n=$\frac{m}{M}$计算出10g丁烷的物质的量,然后计算出1mol丁烷燃烧生成二氧化碳和液态水放出的热量,结合化学方程式对应的物质的量计算反应放出的热量,依据热化学方程式书写方法,标注物质聚集状态和反应焓变写出.
解答 解:解:当10kg丁烷完全反应物质的量:$\frac{10g}{58g/mol}$=$\frac{5}{29}$mol,完全燃烧并生成二氧化碳和液态水时,放出热量为500kJ,
则1mol丁烷完全反应放热为:500kJ×$\frac{1mol}{\frac{5}{29}mol}$=2900kJ,则该反应的热化学方程式为:C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol,
故答案为:C4H10(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2900kJ/mol.
点评 本题考查了热化学方程式的书写,题目难度不大,明确热化学方程式的书写原则为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.在盛有稀硫酸的烧杯中,放入用导线连接的铜片和锌片,下列说法正确的是( )
| A. | 一段时间负极质量明显减轻 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 只有正极上有氢气逸出,正极电极反应式为:2H++2e-═H2↑ | |
| D. | 正极附近的SO42-离子浓度逐渐增大 |
20.下列性质递变规律错误的是( )
| A. | 金属性:K>Na>Li | B. | 酸性:HClO3>H2SO4>H3PO4 | ||
| C. | 还原性:I->Br->Cl- | D. | 氧化性:F2>Cl2>Br2 |
4.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示其中Y所处的周期序数与族序数相等.按要求回答下列问题:
(1)写出X的原子结构示意图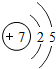 .
.
(2)列举一个事实说明X非金属性强于Z:2HNO3+Na2SiO3=2NaNO3+H2SiO3↓;(用化学方程式表示)
(3)含Y的氯化物呈酸性的原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式表示)
| X | ||||
| Y | Z | W |
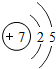 .
.(2)列举一个事实说明X非金属性强于Z:2HNO3+Na2SiO3=2NaNO3+H2SiO3↓;(用化学方程式表示)
(3)含Y的氯化物呈酸性的原因是Al3++3H2O?Al(OH)3+3H+(用离子方程式表示)
14.下列物质晶体结构中含有正四面体结构的化合物是( )
| A. | SiO2 | B. | 金刚石 | C. | KCl | D. | 干冰 |
1.表是A、B、C、D、E五种有机物的有关信息.
(1)A~E中,属于烃的是AB(填字母).
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)C催化氧化生成D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(4)有机物B具有的性质是②③ (填序号).
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O(用化学方程式说明).
| A | ①能使溴的四氯化碳溶液褪色 ②比例模型为 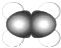 ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成 ②球棍模型为 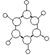 |
| C | ①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C少2 ②能由C催化氧化得到 |
| E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊试液变红 |
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)C催化氧化生成D的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
(4)有机物B具有的性质是②③ (填序号).
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O(用化学方程式说明).
18.按要求选用合适的试剂或操作完成下列的鉴别、分离或除杂.
| 试剂或操作 | |
| 鉴别乙醇和乙酸 | 紫色石蕊试液(Na2CO3溶液、NaHCO3溶液) |
| 鉴别棉花和蚕丝 | 灼烧 |
| 除去乙烷中混有的乙烯 | 溴水(溴的CCl4溶液) |
| 除去苯中溶解的溴单质 | NaOH溶液 |
| 海水淡化 | 蒸馏 |
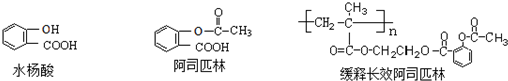
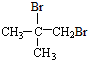 .
.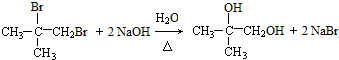 ;
;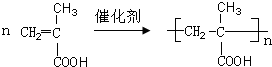 .
.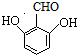 、
、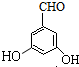 、
、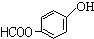 (任写一个).
(任写一个).