题目内容
3. 甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途.
甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途.已知:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-25kJ•mol-1,某温度下的平衡常数为400.此温度下,在1L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol•L-1) | 0.8 | 1.24 | ? |
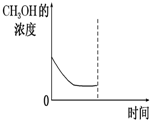
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图.
分析 ①由表中数据可知,CH3OH的起始浓度为0.8mol/L+2×1.24mol/L=3.28mol/L,令平衡后c(CH3OCH3)=xmol/L,根据方程式可知平衡时c(CH3OH)=(3.28-2x)mol/L,c(H2O)=xmol/L,代入平衡常数k=$\frac{c(C{H}_{3}OC{H}_{3})c({H}_{2}O)}{{c}^{3}(C{H}_{3}OH)}$计算;反应混合物的总能量减少等于反应放出的热量,根据B计算中可知生成的n(CH3OCH3),结合热化学方程式计算放出的热量;
②平衡时,再加入与起始等量的CH3OH,等效为增大压强,反应前后气体的物质的量不变,与原平衡等效,平衡后CH3OH转化率不变,以此解答该题.
解答 解:①由表中数据可知,CH3OH的起始浓度为0.8mol/L+2×1.24mol/L=3.28mol/L,令平衡后c(CH3OCH3)=xmol/L,根据方程式可知平衡时c(CH3OH)=(3.28-2x)mol/L,c(H2O)=xmol/L,所以$\frac{{x}^{2}}{(3.28-2x)^{2}}$=400,解得x=1.6mol/L,
反应混合物的总能量减少等于反应放出的热量,由B中可知,平衡时后c(CH3OCH3)=1.6mol/L,所以平衡时n(CH3OCH3)=1.6mol/L×1L=1.6mol,由热化学方程式可知反应放出的热量为25kJ/mol×1.6mol=40kJ,故平衡时,反应混合物的总能量减少40kJ,
故答案为:1.6;40;
②平衡时,再加入与起始等量的CH3OH,等效为增大压强,反应前后气体的物质的量不变,与原平衡等效,平衡后CH3OH转化率不变,浓度为原平衡的2倍,如图 ,故答案为:
,故答案为: .
.
点评 本题考查化学平衡常数的有关计算与影响因素、化学平衡移动、等效平衡、化学反应中能量变化等,难度中等,根据化学平衡常数进行计算.

 一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )
一个密闭容器,中间有一可自由滑动的隔板(厚度不计)将容器分成两部分,当左边充入1molN2,右边充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )| A. | 右边与左边分子数之比为4:1 | |
| B. | 右侧CO的质量为5.6 g | |
| C. | 右侧气体密度是相同条件下氢气密度的14倍 | |
| D. | 若改变右边CO的充入量而使隔板处于容器正中间,保持温度不变,则应充入0.2molCO |
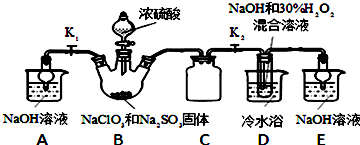
 某兴趣小组设计“氯气与金属钠反应”的装置.实验操作:先给钠预热,到钠熔融成圆球时,停止加热,通入氯气,即可见钠着火燃
某兴趣小组设计“氯气与金属钠反应”的装置.实验操作:先给钠预热,到钠熔融成圆球时,停止加热,通入氯气,即可见钠着火燃烧,并产生大量白烟.以下叙述错误的是( )
| A. | 钠着火燃烧产生苍白色火焰和白烟 | |
| B. | 白烟是氯化钠微晶分散在空气中形成 | |
| C. | 玻管中部塞一团浸有NaOH溶液的棉球是为了吸收过量的氯气,以防污染环境 | |
| D. | 根据管右端棉球颜色的变化情况,可判断氯气是否被碱液完全吸收 |
CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚;浓硫酸把乙醇氧化为CO2等.
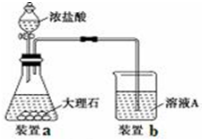
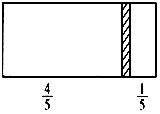
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/°C | 78.5 | 132 | 34.6 |
| 熔点/°C | -130 | 9 | -116 |
(1)A装置上方使用滴液漏斗的优点是:便于漏斗内的液体是顺利滴下;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(2)B装置的作用是平衡压强,检测装置是否发生堵塞.
(3)在装置C中应加入c(填正确选项前的字母),其目的是吸收反应生成的SO2等酸性气体.
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去.
(5)D装置具支试管内若用溴水代替液溴(假定产物相同),分析其优点产物1,2-二溴乙烷和水不互,溶分层,水在上层起着液封,防止产品挥发的作用.
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯和溴单质反应放出热量,冷却可以避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的熔点为9℃,过度冷却会变成固体而使进气导管堵塞.
 )为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |
在圆底烧瓶中加入12.2g苯甲酸(M=122g/mol)和20ml甲醇(密度约0.79g•mL-1 ),再小心加入3mL浓硫酸,混匀后,投入几粒碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品.
(1)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式C6H5CO18OH+CH3OH $\frac{\underline{\;浓硫酸\;}}{△}$C6H5COOCH3+H218O;浓硫酸的作用是:催化剂、吸水剂.
(2)甲、乙、丙三位同学分别设计了如图三套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去).根据有机物的沸点,最好采用乙装置(填“甲”或“乙”或“丙”).
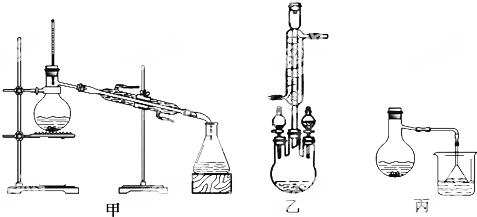
Ⅱ.粗产品的精制
(3)苯甲酸甲酯粗产品中往往含有少量甲醇、硫酸、苯甲酸和水等,现拟用下列流程进行精制,请根据流程图写出操作方法的名称.操作Ⅰ分液 操作Ⅱ蒸馏.

(4)能否用NaOH溶液代替饱和碳酸钠溶液?否(填“能”或“否”),并简述原因氢氧化钠是强碱,促进苯甲酸甲酯的水解,导致产品损失.
(5)通过计算,苯甲酸甲酯的产率是65% .
Ⅰ.(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成为CaO•3MgO•4SiO2.
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)nCl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为+3.
Ⅱ.高纯二氧化硅可用来制造光纤.某稻壳灰的成分如下表:
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.61 |
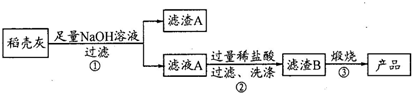
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物的种类最多有3类,其中SiO2为酸性氧化物(填氧化物的类别)
(2)滤渣A的成分有C和Fe2O3填化学式)
(3)步骤②洗涤沉淀的方法是向漏斗中加水至浸没沉淀,待水自然流下后,再重复2-3次
(4)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚钳和三脚架.
| A. | 12C和13C为不同核素 | B. | 金刚石和C60互为同素异形体 | ||
| C. | 1H2和2H2互为同位素 | D. | 氧原子(18O)的结构示意图为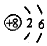 |