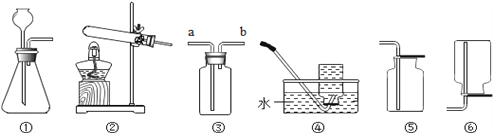
【题目】随州市某初中学校九年级化学兴趣小组学完“盐的性质”后进行下图两个实验。
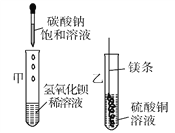
(1)甲实验中反应的化学方程式为__________________。
(2)乙实验观察到的现象是________________________。
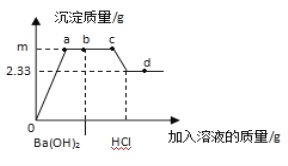
(3)把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(作出猜想)白色沉淀为:Ⅰ._____________;
Ⅱ.Mg(OH)2和BaSO4;Ⅲ. Mg(OH)2和MgCO3。
(实验方案)请你设计一种实验方案证明猜想Ⅲ成立。
实验操作 | 实验现象与结论 |
_________________ | _____________________,猜想Ⅲ成立。有关化学反应方程式为:(写一个即可)________________。 |
(拓展与思考)如果猜想Ⅱ成立,产生此结果的原因是做甲实验时__________________;上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是____________。
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如图.下列说法错误的是( )

温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
A. 乙为NH4Cl
B. t3应介于40℃﹣50℃
C. 55℃时,分别将两饱和溶液蒸发等质量的水,得到固体质量甲>乙
D. 等质量的甲、乙饱和溶液从t3降温到t1,析出的晶体质量相等