题目内容
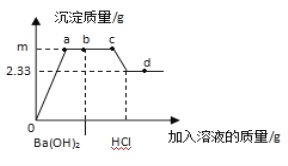
【题目】向CuSO4溶液中先后逐滴滴加100g Ba(OH)2溶液与一定量的HCl溶液,反应过程中加入溶液的质量与产生沉淀质量关系如图所示。下列说法正确的是
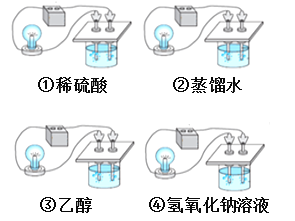
A. o~a溶液导电性逐渐增强
B. d点溶质的成分为一种
C. m=3.31
D. 原Ba(OH)2溶液的溶质质量分数为1.71%
【答案】C
【解析】向CuSO4溶液中先后逐滴滴加过量Ba(OH)2溶液生成BaSO4和Cu(OH)2沉淀,完全反应后再滴加稀盐酸,先中和多余的Ba(OH)2溶液,再溶解Cu(OH)2沉淀,最后剩余BaSO4沉淀;
A.o~a段发生反应为Ba(OH)2+CuSO4===BaSO4↓+Cu(OH)2↓,可知此段溶液导电性逐渐减弱,故A错误;B.d点溶液为过量盐酸与Ba(OH)2溶液、Cu(OH)2沉淀反应后的混合液,溶质为BaCl2、CuCl2及HCl,故B错误;C.设生成的Cu(OH)2沉淀质量为x,
Ba(OH)2+CuSO4===BaSO4↓+Cu(OH)2↓
233 98
2.33g x
![]() ,解得:x=0.98g,则m=2.33g+0.98g=3.31g,故C正确;D.Ba(OH)2溶液过量,未完全与CuSO4溶液反应,无法计算出Ba(OH)2溶液溶质的质量,即溶液的质量分数无法确定,故D错误;答案为C。
,解得:x=0.98g,则m=2.33g+0.98g=3.31g,故C正确;D.Ba(OH)2溶液过量,未完全与CuSO4溶液反应,无法计算出Ba(OH)2溶液溶质的质量,即溶液的质量分数无法确定,故D错误;答案为C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目