5.在我们初中科学中有大量的“既可以…又可以…”的结论.判断下列结论中,与如图示不符合的结论的是( )
| A. |  如图装置既可以收集气体,又可以干燥气体 | |
| B. |  如图装置既可以省力,又可以改变力的方向 | |
| C. |  如图生物既可以光合作用,又可以呼吸作用 | |
| D. |  如图气体既可以助燃,又可以燃烧 |
19.水是人类最宝贵的自然资源,近年在我国已经发生多起饮用水污染事件,水资源的不断污染会给人类造成灾难.某学习小组采集了某河流的水样,并对水样进行以下实验检测:
若水样中可能含有CuSO4、FeCl3、Na2CO3、NaCl、H2SO4中一种或几种,试根据实验分析水样中一定含有的物质是FeCl3、H2SO4;该学习小组同学经分析认为该水样中不含Na2CO3,请用化学方程式表示他们得出该结论的依据:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O.
| 实验内容和步骤 | 实验现象 |
| ①观察水样 | 浅黄色 |
| ②取少量水样,滴加过量的稀硝酸和硝酸钡溶液 | 有白色沉淀产生 |
| ③另取少量水样,用pH试纸检测 | pH=3 |
18.氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是( )


| A. | Fe2O3+3CO$\frac{\underline{\;\;△\;\;}}{\;}$ 2Fe+3CO2 | B. | 2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑ | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | FeCl3+3NaOH═Fe(OH)3↓+3NaCl |
17.关于酸、碱、盐及氧化物,下列说法正确的是( )
0 167007 167015 167021 167025 167031 167033 167037 167043 167045 167051 167057 167061 167063 167067 167073 167075 167081 167085 167087 167091 167093 167097 167099 167101 167102 167103 167105 167106 167107 167109 167111 167115 167117 167121 167123 167127 167133 167135 167141 167145 167147 167151 167157 167163 167165 167171 167175 167177 167183 167187 167193 167201 211419
| A. | pH为3的盐酸溶液加水稀释,可以配成pH为2的盐酸溶液 | |
| B. | 氧化物一定含有氧元素,但含氧元素的物质不一定都是氧化物 | |
| C. | 固体氢氧化钠需密封保存是为了避免它与空气中的水蒸气发生化学反应而潮解 | |
| D. | 酸、碱、盐在水溶液里都可以离解成自由移动的离子,如氢氧化铁可以使紫色石蕊变蓝 |
 如图“五连环”中的每一环表示一种物质,在一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应.请回答:
如图“五连环”中的每一环表示一种物质,在一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应.请回答:
 一定质量的细铁丝(假设不含不杂质)在氧气中完全燃烧后生成四氧化三铁.固体的质量随时间的变化关系如图所示,试计算:
一定质量的细铁丝(假设不含不杂质)在氧气中完全燃烧后生成四氧化三铁.固体的质量随时间的变化关系如图所示,试计算:
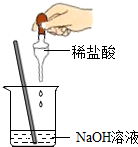 酸与碱作用生成盐和水的反应叫做中和反应,探究中和反应是否发生或酸和碱是否恰好完全反应的方法有多种.某学习小组的同学从不同角度进行有关中和反应的实验探究:
酸与碱作用生成盐和水的反应叫做中和反应,探究中和反应是否发生或酸和碱是否恰好完全反应的方法有多种.某学习小组的同学从不同角度进行有关中和反应的实验探究: